题目内容
在120℃时,将2L H2O、1L N2、1L CO、1L O2和2L CO2组成的混合气体依次缓缓通过过量的热铜粉,过量过氧化钠和过量炽热木炭粉的三个反应管.经充分反应后,恢复到原来温度和压强.其气体体积是
- A.2.5L
- B.3.5L
- C.5L
- D.6L
D
分析:混合气体通过过量的热铜粉,发生反应2Cu+O2=2CuO,CuO+CO=Cu+CO2,相当于O2+2CO=2CO2,2Cu+O2=2CuO,混合气体中1
LCO、1L O2可以生成CO2为1L,剩余氧气与铜反应,即通过过量的热铜粉出来的气体2LH2O、1L N2和3L CO2;出来气体通过过量过氧化钠,发生反应2H2O+2Na2O2=4NaOH+O2,2CO2+2Na2O2=2Na2CO3+O2,水、二氧化碳完全反应,生成氧气2.5L,即通过过量过氧化钠,出来的气体1L N2和2.5LO2;再通过过量炽热的木炭粉,发生反应O2+2C=2CO,生成CO为5L,即通过过量炽热的木炭粉,最终出来的气体为1L1L N2和5LCO.
解答:混合气体通过过量的热铜粉,发生反应2Cu+O2=2CuO,CuO+CO=Cu+CO2,相当于O2+2CO=2CO2,2Cu+O2=2CuO,混合气体中1LCO、1L O2,可以生成V(CO2)=V(CO)=1L,剩余氧气与铜反应,水、氮气未反应,出来气体中二氧化碳为2L+1L=3L,即通过过量的热铜粉出来的气体2LH2O、1L N2和3L CO2;
出来气体通过过量过氧化钠,发生反应2H2O+2Na2O2=4NaOH+O2,2CO2+2Na2O2=2Na2CO3+O2,水、二氧化碳完全反应,由方程式可知,生成氧气V(O2)= V(CO2)+
V(CO2)+ V(H2O)=
V(H2O)= ×3L+
×3L+ ×2L=2.5L,即通过过量过氧化钠,出来的气体1L N2和2.5L
×2L=2.5L,即通过过量过氧化钠,出来的气体1L N2和2.5L
O2;再通过过量炽热的木炭粉,发生反应O2+2C=2CO,由方程式可知生成一氧化氮V(CO)=2V(O2)=2.5L×2=5L,即通过过量炽热的木炭粉,最终出来的气体为1L1L N2和5LCO.即气体体积为1l+5L=6L.
故选:D.
点评:考查根据方程式的反应,难度不大,涉及反应过程较多,清楚反应过程是关键,注意水是气态.
分析:混合气体通过过量的热铜粉,发生反应2Cu+O2=2CuO,CuO+CO=Cu+CO2,相当于O2+2CO=2CO2,2Cu+O2=2CuO,混合气体中1
LCO、1L O2可以生成CO2为1L,剩余氧气与铜反应,即通过过量的热铜粉出来的气体2LH2O、1L N2和3L CO2;出来气体通过过量过氧化钠,发生反应2H2O+2Na2O2=4NaOH+O2,2CO2+2Na2O2=2Na2CO3+O2,水、二氧化碳完全反应,生成氧气2.5L,即通过过量过氧化钠,出来的气体1L N2和2.5LO2;再通过过量炽热的木炭粉,发生反应O2+2C=2CO,生成CO为5L,即通过过量炽热的木炭粉,最终出来的气体为1L1L N2和5LCO.
解答:混合气体通过过量的热铜粉,发生反应2Cu+O2=2CuO,CuO+CO=Cu+CO2,相当于O2+2CO=2CO2,2Cu+O2=2CuO,混合气体中1LCO、1L O2,可以生成V(CO2)=V(CO)=1L,剩余氧气与铜反应,水、氮气未反应,出来气体中二氧化碳为2L+1L=3L,即通过过量的热铜粉出来的气体2LH2O、1L N2和3L CO2;
出来气体通过过量过氧化钠,发生反应2H2O+2Na2O2=4NaOH+O2,2CO2+2Na2O2=2Na2CO3+O2,水、二氧化碳完全反应,由方程式可知,生成氧气V(O2)=
 V(CO2)+
V(CO2)+ V(H2O)=
V(H2O)= ×3L+
×3L+ ×2L=2.5L,即通过过量过氧化钠,出来的气体1L N2和2.5L
×2L=2.5L,即通过过量过氧化钠,出来的气体1L N2和2.5LO2;再通过过量炽热的木炭粉,发生反应O2+2C=2CO,由方程式可知生成一氧化氮V(CO)=2V(O2)=2.5L×2=5L,即通过过量炽热的木炭粉,最终出来的气体为1L1L N2和5LCO.即气体体积为1l+5L=6L.
故选:D.
点评:考查根据方程式的反应,难度不大,涉及反应过程较多,清楚反应过程是关键,注意水是气态.

练习册系列答案
相关题目
在体积固定的密闭容器中,进行如下化学反应:N2O4(g)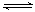 2
NO2(g),其化学平衡常数K和温度t的关系如下表:
2
NO2(g),其化学平衡常数K和温度t的关系如下表:
|
t /℃ |
80 |
100 |
120 |
|
K |
1.80 |
2.76 |
3.45 |
请回答下列问题:
(1)该反应的化学平衡常数表达式K= 。
(2)该反应为 反应(填“吸热”或“放热”)。
(3)判断该反应达到化学平衡状态的依据是 。
A.容器内混合气体密度不变
B.混合气体中c(NO2)不变
C.0.5mol N2O4分解的同时有1 mol NO2生成
(4)在80℃时,将2.80molN2O4气体充入2L固定容积的密闭容器中,一段时间后对该容器内的物质进行分析,得到如下数据:
|
|
0 |
20 |
40 |
60 |
80 |
100 |
|
n(N2O4) |
2.80 |
A |
2.00 |
c |
d |
1.60 |
|
n(NO2) |
0 |
0.96 |
b |
2.08 |
2.40 |
2.40 |
①b的值为 ;
②N2O4的平衡转化率为 ;
③20s~40s内用N2O4表示的平均反应速率υ(N2O4)= 。