题目内容
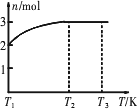
(1)一定温度下,将1 mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色.温度由T1继续升高到T2的过程中,气体逐渐变为无色.若保持T2,增大压强,气体逐渐变为红棕色.气体的物质的量(n)随温度(T)变化的关系如图.
①温度在
T1~T2之间,反应的化学方程式是________;②温度在
T2~T3之间,气体的平均相对分子质量是________(保留1位小数).(2)N2O5是一种新型硝化剂,其性质和制备受到人们的关注.下图所示装置可用于制备N2O5,则N2O5在电解池的________区生成,其电极反应式为________.

答案:
解析:
解析:
|
答案: 讲析: (2)从N2O4变成N2O5可知,N的化合价从+4价变成+5价应发生氧化反应,则应在阳极发生;在书写阳极反应式时要特别注意隔膜阻止水分子通过,所以阳极区的无水硝酸,不能写成离子形式. |

练习册系列答案
相关题目