��Ŀ����
���ִ���ҵ�����Ȼ���Ϊԭ���Ʊ�������ֹ����������£�
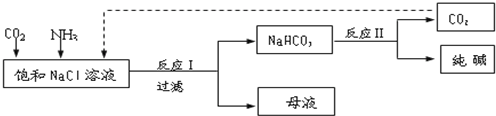
��֪NaHCO3�ڵ������ܽ�Ƚ�С����Ӧ��Ϊ��NaCl+CO2+NH3+H2O
NaHCO3��+NH4Cl������ĸҺ�����ַ������£�
��1����ĸҺ�м���ʯ���飬�ɽ����� ѭ�����ã�
��2����ĸҺ��ͨ��NH3������ϸС��ʳ�ο��������£��ɵõ�NH4Cl���壮��д��ͨ��NH3���ܽ�Ƚ�С����ʽ̼����ת��Ϊ�ܽ�Ƚϴ��̼���ε����ӷ���ʽ ��
��ij��ѧС��ģ�⡰�����Ƽ������NaCl��NH3��CO2��ˮ��Ϊԭ���Լ���ͼ1��ʾװ����ȡNaHCO3��Ȼ���ٽ�NaHCO3�Ƴ�Na2CO3��
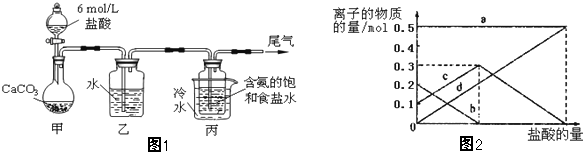
��1��װ�ñ�����ˮ�������� ��
��2����װ�ñ��в�����NaHCO3��ȡNa2CO3ʱ����Ҫ���е�ʵ������� ��ϴ�ӡ����գ�NaHCO3ת��ΪNa2CO3�Ļ�ѧ����ʽΪ ��
��3�����ڣ�2�������յ�ʱ��϶̣�NaHCO3���ֽⲻ��ȫ����С���һ�ݼ�����t1min��NaHCO3��Ʒ����ɽ���������̽����
ȡ������t1min��NaHCO3��Ʒ29.6g��ȫ����ˮ�Ƴ���Һ��Ȼ�������Һ�л����صμ�ϡ���ᣬ�����Ͻ��裮��������ļ��룬��Һ���й����ӵ����ʵ����ı仯��ͼ2��ʾ��
������a��Ӧ����Һ�е������� �������ӷ�����ͬ��������c��Ӧ����Һ�е������� ������Ʒ��NaHCO3��Na2CO3�����ʵ���֮���� ��
��4����ȡ21.0g NaHCO3���壬������t2 rnin��ʣ����������Ϊl4.8g������Ѵ�ʣ�����ȫ�����뵽200mL 2mol?L-1�������У����ַ�Ӧ����Һ��H+�����ʵ���Ũ��Ϊ ������Һ����仯���Բ��ƣ�

��֪NaHCO3�ڵ������ܽ�Ƚ�С����Ӧ��Ϊ��NaCl+CO2+NH3+H2O
| ||
��1����ĸҺ�м���ʯ���飬�ɽ�����
��2����ĸҺ��ͨ��NH3������ϸС��ʳ�ο��������£��ɵõ�NH4Cl���壮��д��ͨ��NH3���ܽ�Ƚ�С����ʽ̼����ת��Ϊ�ܽ�Ƚϴ��̼���ε����ӷ���ʽ
��ij��ѧС��ģ�⡰�����Ƽ������NaCl��NH3��CO2��ˮ��Ϊԭ���Լ���ͼ1��ʾװ����ȡNaHCO3��Ȼ���ٽ�NaHCO3�Ƴ�Na2CO3��

��1��װ�ñ�����ˮ��������
��2����װ�ñ��в�����NaHCO3��ȡNa2CO3ʱ����Ҫ���е�ʵ�������
��3�����ڣ�2�������յ�ʱ��϶̣�NaHCO3���ֽⲻ��ȫ����С���һ�ݼ�����t1min��NaHCO3��Ʒ����ɽ���������̽����
ȡ������t1min��NaHCO3��Ʒ29.6g��ȫ����ˮ�Ƴ���Һ��Ȼ�������Һ�л����صμ�ϡ���ᣬ�����Ͻ��裮��������ļ��룬��Һ���й����ӵ����ʵ����ı仯��ͼ2��ʾ��
������a��Ӧ����Һ�е�������
��4����ȡ21.0g NaHCO3���壬������t2 rnin��ʣ����������Ϊl4.8g������Ѵ�ʣ�����ȫ�����뵽200mL 2mol?L-1�������У����ַ�Ӧ����Һ��H+�����ʵ���Ũ��Ϊ
���㣺���ҵ�������Ƽ��
ר�⣺ʵ����,ʵ�������
������I����1���������̿�֪��ĸҺ�к����Ȼ�泥�����ʯ�����������ɰ�����
��2�����ݰ�ˮ�����笠������������ӣ�����笠���Ũ���������Ȼ�淋���������������Һ������ǿ��ʹ̼������ת��Ϊ�ܽ�Ƚϴ��̼���ƣ�
II����1���¶�Խ�ͣ�NaHCO3���ܽ��ԽС��
��2��װ�ñ����ǰ����ı���ʳ��ˮ��ͨ�������̼����̼�����ƾ��壬ͨ�����˵õ�����ϴ�����յõ�̼���ƣ�NaHCO3ת��ΪNa2CO3�ķ����ǹ�����ȷֽ⣻
��3���������̼���ƺ�̼�����ƣ��������ᷢ����ӦCO32-+H+=HCO3-��HCO3-+H+=CO2��+H2O������ͼ�����̼������Ӽ�С��̼������������ࣻ
��4�����ݷ�Ӧǰ�������仯��̼�����Ʒֽ��ԭ�����ݷ�Ӧǰ�������仯���㷴Ӧ��̼�����ƺ����ɵ�̼���ƣ����������������ʣ��̼�����ƣ�����õ�����ﷴӦ���ĵ������ӵõ���
��2�����ݰ�ˮ�����笠������������ӣ�����笠���Ũ���������Ȼ�淋���������������Һ������ǿ��ʹ̼������ת��Ϊ�ܽ�Ƚϴ��̼���ƣ�
II����1���¶�Խ�ͣ�NaHCO3���ܽ��ԽС��
��2��װ�ñ����ǰ����ı���ʳ��ˮ��ͨ�������̼����̼�����ƾ��壬ͨ�����˵õ�����ϴ�����յõ�̼���ƣ�NaHCO3ת��ΪNa2CO3�ķ����ǹ�����ȷֽ⣻
��3���������̼���ƺ�̼�����ƣ��������ᷢ����ӦCO32-+H+=HCO3-��HCO3-+H+=CO2��+H2O������ͼ�����̼������Ӽ�С��̼������������ࣻ
��4�����ݷ�Ӧǰ�������仯��̼�����Ʒֽ��ԭ�����ݷ�Ӧǰ�������仯���㷴Ӧ��̼�����ƺ����ɵ�̼���ƣ����������������ʣ��̼�����ƣ�����õ�����ﷴӦ���ĵ������ӵõ���
���
�⣺I����1���������з�Ӧ���̿�֪�����˺�õ���ĸҺ�к����Ȼ�泥�ĸҺ�м���ʯ�����Ӧ���ɰ��������������ڷ�Ӧ������ѭ�����ã��ʴ�Ϊ��NH3��
��2����������ˮ�����ɰ�ˮ����ˮ�����笠������������ӣ�����NH4+��Ũ�ȣ������ڳ���ƽ��������NH4Cl�ķ�����У���Һ������ǿ������NaHCO3ת��ΪNa2CO3������������������Ȼ�淋Ĵ��ȣ���Ӧ�����ӷ���ʽΪHCO3-+NH3=NH4++CO32-���ʴ�Ϊ��HCO3-+NH3=NH4++CO32-��
II����1��NaHCO3���ܽ�������¶ȵĽ��Ͷ���С��������ˮ����ʹ��Һ��ȴ������NaHCO3���ܽ�ȣ�ʹ֮�����������ʴ�Ϊ����ȴ��ʹNaHCO3����������
��2����װ�ñ��в�����NaHCO3�����ķ�ӦΪ��NH3+CO2+H2O+NaCl=NaHCO3��+NH4Cl����ȡNa2CO3ʱ��Ҫ���˵õ����壬ϴ�Ӻ�������յõ�̼���ƣ�̼���������ȷֽ����ɶ�����̼��̼���ơ�ˮ����ӦΪ��2NaHCO3
Na2CO3+H2O+CO2����
�ʴ�Ϊ�����ˣ� 2NaHCO3
Na2CO3+H2O+CO2����
��3�����ڣ�2�������յ�ʱ��϶̣�NaHCO3���ֽⲻ��ȫ����С���һ�ݼ�����t1min��NaHCO3��Ʒ����ɽ������о���ȡ������t1min��NaHCO3��Ʒ29.6g ��ȫ����ˮ�Ƴ���Һ��Ȼ�������Һ�л����صμ�ϡ���ᣬ�����Ͻ��裮��������ļ��룬������Ӧ CO32-+H+=HCO3-�� HCO3-+H+=CO2��+H2O����Һ���й����ӵ����ʵ����ı仯Ϊ��̼������Ӽ�С��̼���������Ũ������̼�������ȫ��ת��Ϊ̼��������ӣ��ٵ��������̼��������ӷ�Ӧ���ɶ�����̼��̼��������Ӽ�С���ڴ˹����У�Na+�����뷴Ӧ��Ũ��һֱ���䣬��a���߱�ʾ����Na+Ũ�ȵı仯������c���߱�ʾ����̼���������Ũ�ȱ仯��̼�������Ũ��0.2mol/L��̼���������Ũ��Ϊ0.1mol/L����Ʒ��NaHCO3��Na2CO3�����ʵ���֮����1��2��
�ʴ�Ϊ��Na+��HCO3-��1��2��
��4����ȡ21g NaHCO3�������ʵ���=
=0.25mol��������t1min��ʣ����������Ϊ14.8g��
2NaHCO3=Na2CO3+CO2��+H2O��m
2 1 62
0.2mol 0.1mol 21g-14.8g
��Ӧ��NaHCO3���ʵ���=0.25mol-0.2mol=0.05mol��NaHCO3+HCl=NaCl+H2O+CO2���������Ȼ������ʵ���0.05mol��
Na2CO3���ʵ���=0.1mol��Na2CO3+2HCl=2NaCl+H2O+CO2���������Ȼ������ʵ���0.2mol��ʣ���Ȼ������ʵ���=0.200L��2mol/L-0.05mol-0.2mol=0.15mol��ʣ����Һ��c��H+��=
=0.75mol/L��
�ʴ�Ϊ��0.75mol/L��
��2����������ˮ�����ɰ�ˮ����ˮ�����笠������������ӣ�����NH4+��Ũ�ȣ������ڳ���ƽ��������NH4Cl�ķ�����У���Һ������ǿ������NaHCO3ת��ΪNa2CO3������������������Ȼ�淋Ĵ��ȣ���Ӧ�����ӷ���ʽΪHCO3-+NH3=NH4++CO32-���ʴ�Ϊ��HCO3-+NH3=NH4++CO32-��
II����1��NaHCO3���ܽ�������¶ȵĽ��Ͷ���С��������ˮ����ʹ��Һ��ȴ������NaHCO3���ܽ�ȣ�ʹ֮�����������ʴ�Ϊ����ȴ��ʹNaHCO3����������
��2����װ�ñ��в�����NaHCO3�����ķ�ӦΪ��NH3+CO2+H2O+NaCl=NaHCO3��+NH4Cl����ȡNa2CO3ʱ��Ҫ���˵õ����壬ϴ�Ӻ�������յõ�̼���ƣ�̼���������ȷֽ����ɶ�����̼��̼���ơ�ˮ����ӦΪ��2NaHCO3
| ||
�ʴ�Ϊ�����ˣ� 2NaHCO3
| ||
��3�����ڣ�2�������յ�ʱ��϶̣�NaHCO3���ֽⲻ��ȫ����С���һ�ݼ�����t1min��NaHCO3��Ʒ����ɽ������о���ȡ������t1min��NaHCO3��Ʒ29.6g ��ȫ����ˮ�Ƴ���Һ��Ȼ�������Һ�л����صμ�ϡ���ᣬ�����Ͻ��裮��������ļ��룬������Ӧ CO32-+H+=HCO3-�� HCO3-+H+=CO2��+H2O����Һ���й����ӵ����ʵ����ı仯Ϊ��̼������Ӽ�С��̼���������Ũ������̼�������ȫ��ת��Ϊ̼��������ӣ��ٵ��������̼��������ӷ�Ӧ���ɶ�����̼��̼��������Ӽ�С���ڴ˹����У�Na+�����뷴Ӧ��Ũ��һֱ���䣬��a���߱�ʾ����Na+Ũ�ȵı仯������c���߱�ʾ����̼���������Ũ�ȱ仯��̼�������Ũ��0.2mol/L��̼���������Ũ��Ϊ0.1mol/L����Ʒ��NaHCO3��Na2CO3�����ʵ���֮����1��2��
�ʴ�Ϊ��Na+��HCO3-��1��2��
��4����ȡ21g NaHCO3�������ʵ���=
| 21g |
| 84g/mol |
2NaHCO3=Na2CO3+CO2��+H2O��m
2 1 62
0.2mol 0.1mol 21g-14.8g
��Ӧ��NaHCO3���ʵ���=0.25mol-0.2mol=0.05mol��NaHCO3+HCl=NaCl+H2O+CO2���������Ȼ������ʵ���0.05mol��
Na2CO3���ʵ���=0.1mol��Na2CO3+2HCl=2NaCl+H2O+CO2���������Ȼ������ʵ���0.2mol��ʣ���Ȼ������ʵ���=0.200L��2mol/L-0.05mol-0.2mol=0.15mol��ʣ����Һ��c��H+��=
| 0.15mol |
| 0.2L |
�ʴ�Ϊ��0.75mol/L��
���������⿼���˹�ҵ�ƴ����ԭ�����������������е����ʱ仯�������ɷֵķ����жϺͼ���Ӧ�ã�ʵ����̷��������Ӳ�����β�����գ�ͼ���������жϣ���Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 ������ÿ�ʱ�Ż���ҵϵ�д�
������ÿ�ʱ�Ż���ҵϵ�д�
�����Ŀ
������ij�ֺϳ��л��߷��ӻ������֪����-66�Ľṹ��ʽΪ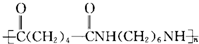 ��
��
�䵥��Ľṹ��ʽӦΪ��������
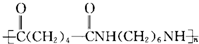 ��
���䵥��Ľṹ��ʽӦΪ��������
| A��HOOCCH2CH2CH2CH2CH2CH2COOH��H2NCH2CH2CH2CH2CH2CH2NH2 |
| B��HOOCCH2CH2CH2CH2CH2CH2COOH��H2NCH2CH2CH2CH2NH2 |
| C��HOOCCH2CH2CH2CH2CH2CH2NH2 |
| D��HOOCCH2CH2CH2CH2COOH��H2NCH2CH2CH2CH2CH2CH2NH2 |
����������ȷ���ǣ�������
| A��ϡ��Ũ����ʱ��Ӧ������ˮ�ز���������ע��Ũ������ |
| B��������Һʱ������ˮ��������ƿ�̶ȣ�Ӧ�ý�ͷ�ιܽ�������Һ���� |
| C����Һʱ����Һ©�����²�Һ����¿ڷų����ϲ�Һ����Ͽڵ��� |
| D���ӵ�ˮ����ȡ���ʵ�ʱ����������ˮ�Ҵ�����CCl4 |
þȼ�ϵ����þ�Ͻ���Ϊ��ص�һ������һ������������⣬�������Һ���ữ���Ȼ�����Һ���ŵ�ʱ�ܷ�Ӧ����ʽ��Mg+2H++H2O2�TMg2++2H2O�����ڸõ��˵����ȷ���ǣ�������
| A��þ�Ͻ�Ϊ��ظ�����������ԭ��Ӧ |
| B���ŵ�ʱH2O2��������Ӧ�õ��� |
| C��������ӦʽΪ��Mg-2e-�TMg2+ |
| D���ŵ�ʱ����������������ǿ |
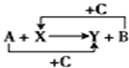 ��֪A��B��C�ǵ�����C����ɫֲ�������õIJ���֮һ��X��Y�ǻ��������֮���ת����ϵ��ͼ����Ӧ�����ԣ�������A��B��Ķ�Ӧ��ϵ������ȷ���ǣ�������
��֪A��B��C�ǵ�����C����ɫֲ�������õIJ���֮һ��X��Y�ǻ��������֮���ת����ϵ��ͼ����Ӧ�����ԣ�������A��B��Ķ�Ӧ��ϵ������ȷ���ǣ�������| A��A������B���� |
| B��A��̼��B�ǹ� |
| C��A��������B��ͭ |
| D��A���ƣ�B������ |
���и���������ָ����Һ���ܴ���������ǣ�������
| A������FeCl3��Һ��I-��NH4+��Cl-��Ba2+ |
| B��������Һ�У�Fe2+��Al3+��NO3-��Cl- |
| C����ɫ��Һ�У�K+��Na+��MnO4-��SO42- |
| D�������Ƶ���Һ�У�Mg2+��K+��HCO3- |