题目内容
将等物质的量的A、B混合放于5L的密闭容器中,发生反应3A(g)+B(g)?xC(g)+2D(g).经5min后测得D的浓度为0.5mol?L-1,c(A):c(B)=3:5,v(C)=0.05mol?L-1?min-1.
则:(1)x= .
(2)前5min内A的反应速率v(A)= .
(3)5min时A的转化率为 .
则:(1)x=
(2)前5min内A的反应速率v(A)=
(3)5min时A的转化率为
考点:反应速率的定量表示方法
专题:
分析:先设A、B的物质的量为nmol;根据D的浓度计算D的物质的量,根据D的物质的量计算反应的A、B的物质的量,根据5min时,A、B浓度之比求出A、B开始时的物质的量,用开始时的物质的量减反应的物质的量即为5min末的物质的量,再根据物质的量浓度公式计算浓度;反应速率之比即为计量数之比;根据C的反应速率求A的反应速率.根据A的转化浓度计算A的转化率.
解答:
解:D的浓度为0.5mol/L,所以D的物质的量为1mol.
设A、B的物质的量为nmol,
3A(g)+B(g)=xC(g)+2D(g),
开始 n mol n mol 0 0
反应 1.5mol 0.5mol 1mol
5min (n-1.5)mol ( n-0.5)mol 1mol
同一容器中,c(A):c(B)=n(A):n(B)=
=
;n=3mol;
(1)D的浓度为0.5mol/L,反应时间为5min,D的反应速率为
=0.1mol/(L?min),C的反应速率是0.05mol/(L?min),根据同一反应中,各物质的反应速率之比等于计量数之比,所以x=1,故答案为:1;
(2)C的反应速率是0.05mol/(L?min),根据同一反应中,各物质的反应速率之比等于计量数之比,所以A的反应速率是3×0.05mol/(L?min)=0.15mol/(L?min),
故答案为:0.15mol/(L?min);
(3)A的转化率为:
×100%=50%,故答案为:50%.
设A、B的物质的量为nmol,
3A(g)+B(g)=xC(g)+2D(g),
开始 n mol n mol 0 0
反应 1.5mol 0.5mol 1mol
5min (n-1.5)mol ( n-0.5)mol 1mol
同一容器中,c(A):c(B)=n(A):n(B)=
| n-1.5 |
| n-0.5 |
| 3 |
| 5 |
(1)D的浓度为0.5mol/L,反应时间为5min,D的反应速率为
| 0.5mol/L |
| 5min |
(2)C的反应速率是0.05mol/(L?min),根据同一反应中,各物质的反应速率之比等于计量数之比,所以A的反应速率是3×0.05mol/(L?min)=0.15mol/(L?min),
故答案为:0.15mol/(L?min);
(3)A的转化率为:
| 1.5mol |
| 3mol |
点评:本题考查了化学反应速率与化学计量数的关系,根据反应物的物质的量关系运用三段式法计算平衡时的物质的量是解答该题的关键,注意同一反应中反应速率之比等于化学计量数之比.

练习册系列答案
相关题目
某无色溶液既可能是强酸性又可能是强碱性,在该溶液中一定能大量共存的离子是( )
| A、H+ Na+ NO3- SO42- |
| B、Na+ CO32- Cu2+ Cl- |
| C、K+ Na+ Cl- SO42- |
| D、K+ Cl- Ba2+ HCO3- |
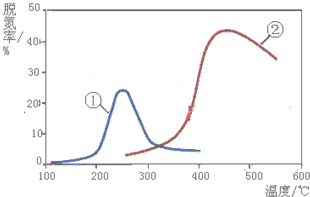
采用NH3作还原剂,除去烟气中的氮氧化物,反应原理为:NO(g)+NO2(g)+2NH3(g)?2N2(g)+3H2O(g).如图是烟气以固定的流速通过两种不同催化剂①和②时,测量相同时间得到的烟气脱氮率图象.根据该图象,下列说法中正确的是( )

| A、上述反应的正反应为吸热反应 |
| B、催化剂①、②分别适合于250℃和450℃左右脱氮 |
| C、催化剂②比①脱氮效果好,说明催化剂②能导致该反应平衡向右移动程度更大 |
| D、相同条件下,改变压强对脱氮率没有影响 |
可逆反应3A(g)3B+C;△H>0,随着温度升高,气体的平均相对分子质量有变小的变化趋势.下列关于B、C两种物质的聚集状态的判断错误的是( )
| A、B和C可能都是固体 |
| B、B和C可能都是气体 |
| C、B和C一定都是气体 |
| D、若C为固体,则B一定是气体 |
一定条件下Cu2S与稀HNO3发生反应,所得还原产物为NO,氧化产物为Cu2+和SO42-.现将0.06molCu2S加入到50mL、4mol/LHNO3中,充分反应之后,下列说法正确的是( )
| A、被还原的硝酸为0.2mol |
| B、反应后溶液中仍有硝酸剩余 |
| C、反应后溶液的pH=1 (溶液体积不变) |
| D、Cu2S未全部参加反应 |
下列肥料中属于复合肥的是( )
| A、磷酸二氢钙 | B、硝酸钾 |
| C、氨水 | D、硫酸铵 |
 如图为直流电源电解稀Na2SO4溶液的装置.通电一段时间后,在石墨电极a和b附近分别滴加一滴酚酞溶液.则下列有关说法中正确的是( )
如图为直流电源电解稀Na2SO4溶液的装置.通电一段时间后,在石墨电极a和b附近分别滴加一滴酚酞溶液.则下列有关说法中正确的是( )| A、a电极产生H2 |
| B、两极产生的气体均有刺激性气味 |
| C、通电一段时间后,稀Na2SO4溶液酸性增强 |
| D、a电极附近呈无色,b电极附近呈红色 |
下列物质分子的几何构型为三角锥形的是( )
| A、CO2 |
| B、P4 |
| C、NH3 |
| D、H2O |