题目内容
14.工业上可用以下方案使饮用水中N03-含量达标.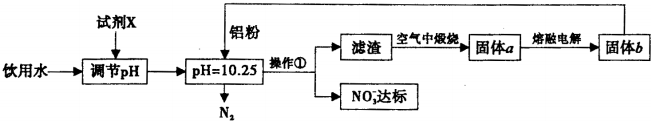
请回答下列问题:
(1)调节pH不宜过大或过小,否则会造成铝的利用率降低;试剂X可选用B(填序号).
A.NaOH B.Ca(OH)2 C.NH3.H2O D.CuO E.CO2
(2)流程中操作①的名称为过滤.
(3)写出溶液中铝粉和NO3-反应的离子方程式:10Al+6NO3-+18H2O═10Al(OH)3↓+3N2↑+6OH-.
(4)还可用以下化学反应使饮用水中NO3-含量达标,产物之一是空气的主要成分.完成下列离子方程式:
□H2+□NO3-+□2H+$\frac{\underline{\;催化剂\;}}{\;}$□N2+□H2O.
分析 试剂X为Ca(OH)2,选用Ca(OH)2调节pH,原料来源丰富,价格便宜,且引人离子对人体无害,在pH=10.25时加入铝粉,与NO3-发生氧化还原反应生成氮气和氢氧化铝,煅烧生成氧化铝,电解可生成铝,
(1)pH过大或过小,加入的铝粉会反应生成H2,造成Al的利用率降低.选用Ca(OH)2调节pH较合适,因引入的Ca2+对人体无害,且来源丰富,价格便宜.
(2)操作①是过滤.
(3)根据流程的信息可知,铝粉还原溶液中NO3-生成N2,同时生成难溶物Al(OH)3.
(4)H2还原NO3-也生成N2(空气的主要成分).
解答 解:试剂X为Ca(OH)2,选用Ca(OH)2调节pH,原料来源丰富,价格便宜,且引人离子对人体无害,在pH=10.25时加入铝粉,与NO3-发生氧化还原反应生成氮气和氢氧化铝,煅烧生成氧化铝,电解可生成铝,
(1)选用熟石灰调节pH,原料来源丰富,价格便宜,且引人离子对人体无害,注意pH过大或过小,都将直接发生Al与酸或碱的反应,否则会造成Al的大量消耗,
故答案为:铝;B;
(2)流程中操作①用于分离固体和液体,为过滤操作,用到的仪器有烧杯、漏斗、玻璃棒,
故答案为:过滤;
(3)铝粉与硝酸根离子发生氧化还原反应生成固体,则固体为氢氧化铝,则硝酸被还原为氮气,则在溶液中铝粉和NO3-反应的离子方程式为10Al+6NO3-+18H2O=10Al(OH)3+3N2↑+6OH-,
故答案为:10Al+6NO3-+18H2O═10Al(OH)3↓+3N2↑+6OH-;
(4)H2催化还原饮用水中NO3-,反应中的还原产物和氧化产物均可参与大气循环,则产物为水和氮气,该反应为5H2+2NO3-+2H+$\frac{\underline{\;催化剂\;}}{\;}$N2+6H2O,
故答案为:5;2;2H+;N2;6.
点评 本题以信息的形式考查氧化还原反应、离子反应,侧重于学生的分析、实验能力的考查,为高频考点和常见题型,注重对化学用语的考查,注意知识与题目信息的结合来解答,对学生能力要求较高,题目难度中等.

 春雨教育同步作文系列答案
春雨教育同步作文系列答案| A. | 某酸性溶液中可能大量存在:NH4+、Fe3+、NO3-、I- | |
| B. | 由水电离的c(H+)=10-12 mol•L-1的溶液中,Al3+、Cl-、Ba2+、NO3-一定不能大量共存 | |
| C. | 向NH3•H2O溶液中滴加少量AlCl3溶液,发生反应:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 向含有1 mol FeBr2的水溶液中通入标准状况下11.2 L Cl2,发生反应:Cl2+2Fe2+═2Fe3++2Cl- |
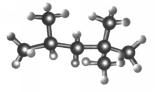 “辛烷值”用来表示汽油的质量,汽油中异辛烷的爆震程度最小,将其辛烷值标定为100,如图是异辛烷的球棍模型,则异辛烷的系统命名为( )
“辛烷值”用来表示汽油的质量,汽油中异辛烷的爆震程度最小,将其辛烷值标定为100,如图是异辛烷的球棍模型,则异辛烷的系统命名为( )| A. | 1,1,3,3-四甲基丁烷 | B. | 2,2,4-甲基庚烷 | ||
| C. | 2,4,4-三甲基戊烷 | D. | 2,2,4-三甲基戊烷 |
| A. | 按系统命名法,化合物 的名称是 2,5,5-三甲基-3-乙基庚烷 的名称是 2,5,5-三甲基-3-乙基庚烷 | |
| B. | 将 与NaOH的醇溶液共热可制备 CH3-CH═CH2 与NaOH的醇溶液共热可制备 CH3-CH═CH2 | |
| C. | 向柠檬醛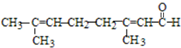 中加入酸性高锰酸钾,若溶液褪色,说明分子中含有醛基 中加入酸性高锰酸钾,若溶液褪色,说明分子中含有醛基 | |
| D. | 葡萄糖与果糖、淀粉与纤维素分子式相同,均互为同分异构体 |
| A. | N2O | B. | N2 | C. | NO | D. | NO2 |
| A. | 1:1:1 | B. | 1:1:3 | C. | 1:3:1 | D. | 3:1:1 |

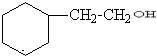 .
.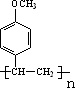 .
.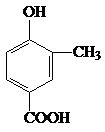 +CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$
+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O.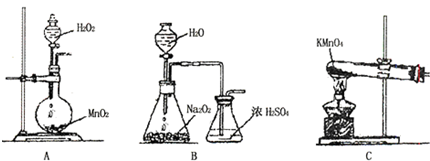
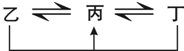 有A、B、C、D、E、F六种前四周期的元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D和F元素对应的单质为日常生活中常见金属.A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e-、空间构型为三角锥形,C元素原子的最外层电子数是其电子层数的3倍,C与E同主族.图中均含D或F元素的物质均会有图示转化关系:
有A、B、C、D、E、F六种前四周期的元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D和F元素对应的单质为日常生活中常见金属.A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e-、空间构型为三角锥形,C元素原子的最外层电子数是其电子层数的3倍,C与E同主族.图中均含D或F元素的物质均会有图示转化关系: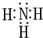 .
.