题目内容
18.现有A、B、C、D、E五种原子序数依次增加的短周期元素.其中A的最低负价和最高正价代数和为零,且A2常温下为气态,B与其他元素形成的化合物种类最多,C与E可形成EC2和EC3两种物质,D是短周期最活泼的金属元素,用化学用语回答下列问题:(1)D离子结构示意图
 ,B在元素周期表的位置第二周期IVA族;
,B在元素周期表的位置第二周期IVA族;(2)A与C形成含18个电子的化合物的电子式是
 ;
;(3)C与D形成的一种化合物颜色为淡黄色,其阴阳离子个数比为1:2,含有的化学键类型为离子键、共价键.
(4)C、D、E的常见离子的离子半径由大到小的顺序S2->O2->Na+;
(5)B、E两元素得电子能力B<E(填“<”或“>”),试写出证明该结论的一个化学方程式H2SO4+2Na2CO3=Na2SO4+CO2↑+H2O;
(6)工业上常用氨水吸收尾气中的EC2,离子方程式为SO2+2NH3﹒H2O=2NH4++SO32-+H2O或SO2+NH3﹒H2O=NH4++HSO3-.
分析 A、B、C、D、E五种原子序数依次增加的短周期元素,其中A的最低负价和最高正价代数和为零且A2常温下为气态,则A为氢元素;B与其他元素形成化合物种类最多,则B为碳元素;C与E可形成EC2和EC3两种物质,则C为O元素、E为S元素;D是短周期最活泼的金属元素,则D为Na,据此解答.
解答 解:A、B、C、D、E五种原子序数依次增加的短周期元素,其中A的最低负价和最高正价代数和为零且A2常温下为气态,则A为氢元素;B与其他元素形成化合物种类最多,则B为碳元素;C与E可形成EC2和EC3两种物质,则C为O元素、E为S元素;D是短周期最活泼的金属元素,则D为Na.
(1)D离子为Na+,离子结构示意图为 ,B为碳元素,在元素周期表的位置:第二周期IVA族,故答案为:
,B为碳元素,在元素周期表的位置:第二周期IVA族,故答案为: ;第二周期IVA族;
;第二周期IVA族;
(2)A与C形成含18个电子的化合物为H2O2,电子式是 ,故答案为:
,故答案为: ;
;
(3)C与D形成的一种化合物颜色为淡黄色为Na2O2,其阴阳离子个数比为1:2,含有的化学键类型为:离子键、共价键,故答案为:1:2;离子键、共价键;
(4)电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大,故离子半径:S2->O2->Na+,故答案为:S2->O2->Na+;
(5)非金属性C<S,故两元素得电子能力C<S,证明该结论的一个化学方程式:H2SO4+2Na2CO3=Na2SO4+CO2↑+H2O,
故答案为:<;H2SO4+2Na2CO3=Na2SO4+CO2↑+H2O;
(6)工业上常用氨水吸收尾气中的SO2,离子方程式为:SO2+2NH3﹒H2O=2NH4++SO32-+H2O 或SO2+NH3﹒H2O=NH4++HSO3-,
故答案为:SO2+2NH3﹒H2O=2NH4++SO32-+H2O 或SO2+NH3﹒H2O=NH4++HSO3-.
点评 本题考查结构性质位置关系运用,推断元素是解题关键,注意对基础知识的理解掌握,掌握金属性、非金属性强弱比较实验事实.

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案| A. | 0.1 mol•L-1 HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+) | |
| B. | 1L0.1mol•L-1 CuSO4•(NH4)2SO4•6H2O的溶液中:c(SO42-)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-) | |
| C. | 常温下,将稀氨水逐滴加入到稀硫酸中,当溶液的pH=7时:c(NH4+)=2c(SO42-) | |
| D. | 等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
| A. | 氢氧化铝是白色胶状沉淀,能凝聚水中的悬浮物,但不能吸附色素 | |
| B. | 不慎将浓碱溶液沾到皮肤上,要立即用大题水冲洗,然后涂上硼酸 | |
| C. | 氮气化学性质通常不活泼,可将炽热的镁粉可放在氮气中冷却 | |
| D. | 酒精灯着火时可用水扑灭 |
| A. | 向沸水中滴加饱和的氯化铁溶液:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3H+ | |
| B. | 向Mg(HCO3)2溶液中加入过量澄清石灰水:Mg2++2HCO3-+2OH-+Ca2+=MgCO3↓+CaCO3↓+2H2O | |
| C. | 氧化铁溶氢碘酸溶液中:Fe2O3+6H++2I-=2Fe2++I2+3H2O | |
| D. | 明矾溶液与Ba(OH)2溶液混合:2Al3++3SO42-+3Ba2++6OH-=3BaSO4↓+2Al(OH)3↓ |
 的混合物与金属钠反应,生成的烷烃不可能是( )
的混合物与金属钠反应,生成的烷烃不可能是( )| A. | CH3CH2CH2CH3 | B. | CH3CH2CH2CH2CH3 | C. | (CH3)2CHCH2CH2CH3 | D. | CH3CH2CH(CH3)2 |
| A. | 切开的金属Na暴露在空气中,光亮表面逐渐变暗2Na+O2═Na2O2 | |
| B. | 少量铜片放入浓硝酸中,有红棕色气体生成:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| C. | Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物2Na2O2+2CO2═2Na2CO3+O2 | |
| D. | 向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |

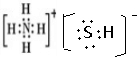 ,写出再生反应的化学方程式:2NH4HS+O2$\frac{\underline{\;一定条件\;}}{\;}$2NH3•H2O+2S;NH3的沸点高于H2S,是因为NH3分子之间存在着一种叫氢键的作用力.
,写出再生反应的化学方程式:2NH4HS+O2$\frac{\underline{\;一定条件\;}}{\;}$2NH3•H2O+2S;NH3的沸点高于H2S,是因为NH3分子之间存在着一种叫氢键的作用力.
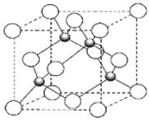 X、Z、Q、R、T为前四周期元素,且原子序数依次增大.X和Q属同族元素,X和R可形成化合物XR4;R2为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;T2+的3d 轨道中有5个电子.请回答下列问题:
X、Z、Q、R、T为前四周期元素,且原子序数依次增大.X和Q属同族元素,X和R可形成化合物XR4;R2为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;T2+的3d 轨道中有5个电子.请回答下列问题: