题目内容
五种短周期元素在周期表中的位置如图所示,其中Z元素原子的最外层电子数等于电子层数。下列判断正确的是
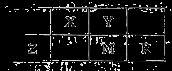
A.Z的氧化物可以做光导纤维
B.气态氢化物稳定性:M>R
C.最高价氧化物对应水化物的酸性:Y>X
D.Z、M、R的原子半径依次增大,最高化合价依次升高
C
【解析】
试题分析:根据题意可知:X是C,Y是N;Z是Al;M是P;R是S。A.Z的氧化物Al2O3可以做冶炼Al,错误;B.元素的非金属性越强,其对应的氢化物的稳定性就越强。由于元素的非金属性:R >M,气态氢化物稳定性:R > M,错误;C.元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强,由于元素的非金属性:Y>M,所以最高价氧化物对应水化物的酸性:Y>X,正确;D.Z、M、R是同一周期的元素,随着原子序数的增大,原子半径逐渐减小,由于原子最外层电子式逐渐增多,所以元素的最高化合价依次升高,错误。
考点:考查元素的推断、元素周期表、元素周期律的应用的知识。

 阅读快车系列答案
阅读快车系列答案(19分) (1)利用H2S废气制取氢气的方法有多种。
①高温热分解法:已知:H2S(g)  H2(g)+1/2S2(g)ΔH在恒容密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为c mol/L测定H2S的转化率,结果见图。
H2(g)+1/2S2(g)ΔH在恒容密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为c mol/L测定H2S的转化率,结果见图。
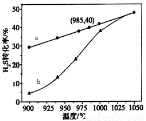
图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。ΔH_____0(填>,=或<):说明随温度的升高,曲线b向曲线a靠近的原因:________________________。
②电化学法:该法制氢过程的示意图如图。
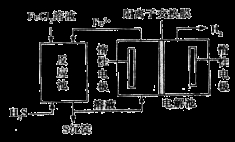
反应池中反应的离子方程式是_____________________________;
反应后的溶液进入电解池,电解总反应的离子方程式为___________________________________。
(2)以Al和NiO(OH)为电极,NaOH溶液为电解液可以组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2。
①该电池的负极反应式__________________。②电池总反应的化学方程式__________________。
(3)某亚硝酸钠固体中可能含有碳酸钠和氢氧化钠,现测定亚硝酸钠的含量。
已知:5NaNO2+2KMnO4+3H2SO4=5NaNO3+2MnSO4+K2SO4+3H2O
称取4.000g固体,溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L,酸性KMnO4溶液进行滴定,实验所得数据如下表所示;
滴定次数 | 1 | 2 | 3 | 4 |
KMnO4溶液的体积/ml | 20.60 | 20.02 | 20.00 | 19.98 |
①滴入最后一滴酸性KMnO4溶液,溶液___________,30秒内不恢复,可判断达到滴定终点。
②第一组实验数据出现异常,造成这种异常的原因可能是____________(填序号)。
A.酸式滴定管用蒸馏水洗净后未用标准液润洗;
B.锥形瓶洗净后未干燥;
C.滴定终了仰视读数
③根据表中数据,计算所得固体中亚硝酸钠的质量分数_____________。
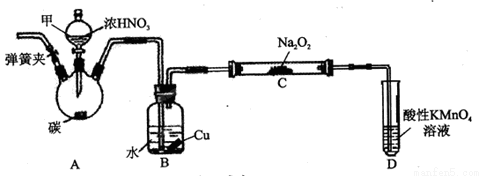

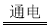 Cu2O+H2↑。下列说法正确的是
Cu2O+H2↑。下列说法正确的是
 CaSiO3+CO2↑的发生,说明硅酸的酸性强于碳酸
CaSiO3+CO2↑的发生,说明硅酸的酸性强于碳酸