题目内容
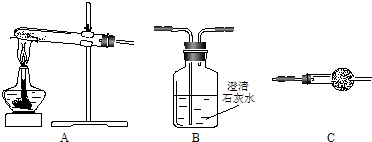
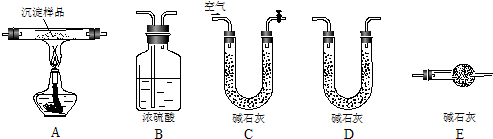
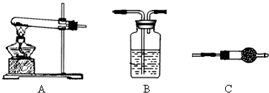
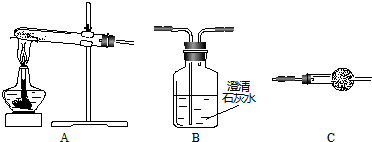
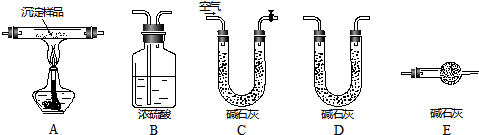
用下图所示装置(必要时可加热试管),不能完成的实验是
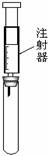
- A.试管中盛酚酞试液,验证氨气的水溶液呈碱性
- B.试管中盛酸性高锰酸钾溶液,探究SO2的还原性
- C.试管中盛稀氢氧化钠溶液,验证CO2与NaOH反应的产物
- D.试管中盛淀粉KI溶液,验证氯气氧化性
C
试题分析:氨气溶于水,生成一水合氨,溶液显碱性。加热时氨气挥发,碱性减弱,A可以;SO2具有还原性,能使酸性高锰酸钾溶液褪色,B正确;CO2和氢氧化钠溶液反应生成碳酸氢钠或碳酸钠,通过该装置无法验证产物,C不正确;氯气能使碘化钾氧化生成单质碘,碘遇淀粉显蓝色,D正确,答案选C。
考点:考查常见物质的性质、检验以及实验设计和评价
点评:该题是高考中的常见考点,属于中等难度的试题,试题设计新颖,有利于调动学生的学习兴趣,激发学生的学习求知欲。该题的关键是记住常见物质的性质,特别是有关物质检验的试剂和实验现象,有利于培养学生的实验设计、操作和评价能力。
试题分析:氨气溶于水,生成一水合氨,溶液显碱性。加热时氨气挥发,碱性减弱,A可以;SO2具有还原性,能使酸性高锰酸钾溶液褪色,B正确;CO2和氢氧化钠溶液反应生成碳酸氢钠或碳酸钠,通过该装置无法验证产物,C不正确;氯气能使碘化钾氧化生成单质碘,碘遇淀粉显蓝色,D正确,答案选C。
考点:考查常见物质的性质、检验以及实验设计和评价
点评:该题是高考中的常见考点,属于中等难度的试题,试题设计新颖,有利于调动学生的学习兴趣,激发学生的学习求知欲。该题的关键是记住常见物质的性质,特别是有关物质检验的试剂和实验现象,有利于培养学生的实验设计、操作和评价能力。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目