题目内容
11.Y元素最高正价与负价的绝对值之差是6;Y元素与M元素形成离子化合物,并在水中电离出电子层结构相同的离子,该化合物是( )| A. | KCl | B. | NaF | C. | Na2O | D. | NaCl |
分析 Y元素的最高正价与负价的代数和为6,最高正价和最低负价的绝对值的代数和为8,由此计算Y元素最高价+7,最低负价-1,Y是第ⅦA族的元素,结合Y离子和M离子相同的电子层结构,逐项判断.
解答 解:Y元素的最高正价与负价的代数和为6,最高正价和最低负价的绝对值的代数和为8,可知Y元素最高价+7,最低负价-1,Y是第ⅦA主族的元素,Y离子和M离子相同的电子层结构,则M位于Y所在周期的下一周期,
A.KCl中钾离子与氯离子电子层结构相同,氯元素处于第ⅦA主族,符合题意,故A正确;
B.NaF中离子有相同的电子层结构,但氟元素没有正化合价,故B错误;
C.Na2O中离子有相同的电子层结构,但氧离子不是第ⅦA主族的元素,故C错误;
D.NaCl中离子的电子层结构不同,氯离子含有三个电子层,钠离子含有两个电子层,故D错误,
故选:A.
点评 本题考查原子结构与性质,题目难度不大,根据最高正价与负价的关系判断Y元素的位置是解题的关键,结合选项再逐一验证,侧重于考查学生的分析能力和应用能力.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案
相关题目
2.Fe3+和I-在水溶液中的反应如下:2I-+2Fe3+?2Fe2++I2(水溶液)
(1)在一定温度下,测得2min内生成I2的物质的量浓度为0.02mol/L,则用Fe3+表示该反应在这2min内平均反应速率为0.02mol•L-1•min-1.
(2)假设c(I-)由0.1mol/L降到0.07mol/L需15s,那么c(I-)由0.07mol/L降到0.05mol/L,所需反应的时间为大于10s(填“大于”、“小于”或“等于”)
(3)上述反应的正反应速率和I-、Fe3+的物质的量浓度关系为:ν=k{c(I-)}m{c(Fe3+)}n(k为常数)
通过上表所给的数据计算,得知:ν=k{c(I-)}m{c(Fe3+)}n中,m、n的值为C(选填A、B、C、D)
A.m=1,n=1 B.m=1,n=2 C.m=2,n=1 D.m=2,n=2
(4)I-物质的量浓度对反应速率的影响大于(填“大于”、“小于”或“等于”)Fe3+物质的量浓度对反应速率的影响.
(1)在一定温度下,测得2min内生成I2的物质的量浓度为0.02mol/L,则用Fe3+表示该反应在这2min内平均反应速率为0.02mol•L-1•min-1.
(2)假设c(I-)由0.1mol/L降到0.07mol/L需15s,那么c(I-)由0.07mol/L降到0.05mol/L,所需反应的时间为大于10s(填“大于”、“小于”或“等于”)
(3)上述反应的正反应速率和I-、Fe3+的物质的量浓度关系为:ν=k{c(I-)}m{c(Fe3+)}n(k为常数)
| C(I-)/(mol•L-1) | C(Fe3+)/(mol•L-1) | ν/(mol•(L•s)-1) | |
| ① | 0.20 | 0.80 | 0.032k |
| ② | 0.60 | 0.40 | 0.144k |
| ③ | 0.80 | 0.20 | 0.128k |
A.m=1,n=1 B.m=1,n=2 C.m=2,n=1 D.m=2,n=2
(4)I-物质的量浓度对反应速率的影响大于(填“大于”、“小于”或“等于”)Fe3+物质的量浓度对反应速率的影响.
19.下列物质中,可一次性鉴别乙酸、乙醇、苯及氢氧化钡溶液的是( )
| A. | 氢氧化钠溶液 | B. | 溴水 | C. | 碳酸钠溶液 | D. | 紫色石蕊溶液 |
6.将100mL 0.001mol•L-1的盐酸和50mL pH=3的硫酸溶液混合后,所得溶液的pH为( )
| A. | 4.5 | B. | 2.7 | C. | 3.3 | D. | 3 |
20.关于${\;}_{92}^{235}$U和${\;}_{92}^{238}$U的说法正确的是( )
| A. | 它们都含有 92个中子 | B. | 235U原子核外有143个电子 | ||
| C. | 它们互为同位素 | D. | 它们是同种核素 |
1.原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1.a-的电子层结构与氦相同,b和c的次外层有8个电子,c-和d+的电子层结构相同.下列叙述错误的是( )
| A. | 元素的非金属性次序为c>b>a | |
| B. | a和其他3种元素均能形成共价化合物 | |
| C. | 元素b、c的气态氢化物的稳定性:b<c | |
| D. | 元素b、c的最高价氧化物对应的水化物的酸性:b>c |
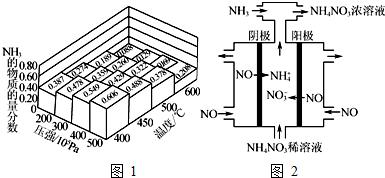
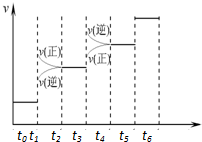 已知N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ•mol-1.请回答:(1)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如右图所示.图中tl时引起平衡移动的条件可能是增大压强.其中表示平衡混合物中NH3的含量最高的一段时是t2-t3.
已知N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ•mol-1.请回答:(1)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如右图所示.图中tl时引起平衡移动的条件可能是增大压强.其中表示平衡混合物中NH3的含量最高的一段时是t2-t3.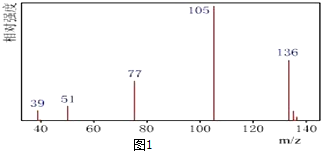
 .
.