题目内容
将A、B以物质的量之比为3:1的比例混合于2L的密闭容器中,发生如下反应:2A(g)+B(g)?xC(g)+D(g),经4min后,测得D的浓度为0.4mol?L-1,A、B物质的量浓度之比为5:1,C的平均反应速率是0.1mol?L-1?min-1.
求:(1)B的转化率是
(2)这4min内 A的平均反应速率为
(3)x值是 .
求:(1)B的转化率是
(2)这4min内 A的平均反应速率为
(3)x值是
考点:化学平衡的计算
专题:化学平衡专题
分析:(1)根据D的浓度求出D的物质的量,结合方程式求出A、B的物质的量,根据物质B的转化率为
;
(2)先求出反应的A的物质的量,再根据平均反应速率公式计算A的平均反应速率;
(3)根据同一反应中反应速率之比等于化学计量数之比求出x值.
| B的变化量 |
| B的起始量 |
(2)先求出反应的A的物质的量,再根据平均反应速率公式计算A的平均反应速率;
(3)根据同一反应中反应速率之比等于化学计量数之比求出x值.
解答:
解:(1)4分钟后,n(D)=CV=0.4mol/L×2L=0.8mol,设反应开始前放入容器中B物质的量为mmol、则A物质的量为3mmol,
2A(g)+B(g)?xC(g)+D(g),
反应前 3m mol m mol 0 0
4分钟后(3m-1.6)mol ( m-0.8)mol 0.8mol
c(A):c(B)=5:1=( 3m-1.6)mol:( m-0.8)mol
m=1.2 mol
4min时物质B的转化率为
=
=66.7%,故答案:66.7%;
(2)由(1)中数据,则A平均反应速率为=
=
=0.2mol?L-1?min-1,故答案为:0.2mol?L-1?min-1;
(3)根据同一反应中反应速率之比等于化学计量数之比,所以v(A):v(C)=0.2mol/(L.min):0.1mol/(L?min)=2:x,所以x=1,故答案为:1.
2A(g)+B(g)?xC(g)+D(g),
反应前 3m mol m mol 0 0
4分钟后(3m-1.6)mol ( m-0.8)mol 0.8mol
c(A):c(B)=5:1=( 3m-1.6)mol:( m-0.8)mol
m=1.2 mol
4min时物质B的转化率为
| B的变化量 |
| B的起始量 |
| 0.8 |
| 1.2 |
(2)由(1)中数据,则A平均反应速率为=
| △C |
| △t |
| ||
| 4min |
(3)根据同一反应中反应速率之比等于化学计量数之比,所以v(A):v(C)=0.2mol/(L.min):0.1mol/(L?min)=2:x,所以x=1,故答案为:1.
点评:本题考查了化学反应速率与化学计量数的关系,明确同一反应中反应速率之比等于化学计量数之比是解(3)的关键.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
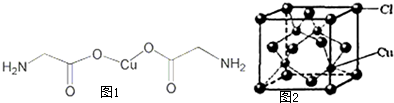
有关下列物质的结构与性质的说法中正确的是( )
| A、NH3 分子的空间构型为平面三角形,是非极性分子 |
| B、过氧化钠属于离子化合物,其晶体中含有非极性共价键 |
| C、水分子间存在氢键,所以水的化学性质稳定 |
| D、H-C≡C-H中的σ键和π键之比为1:2 |
元素中最高正价与负价绝对值的差等于6的是( )
| A、N | B、S | C、Cl | D、Al |
某浓度的硝酸与过量铁粉反应,生成4.48LN2O气体(标准状况).如改与铝反应(生成NO气体),则最后可溶解铝的量是( )
| A、13.5g | B、9g |
| C、27g | D、0.33mol |
硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如图所示).下列说法错误的是( )
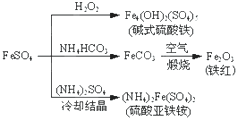

A、FeCO3转化为铁红的化学方程式:4FeCO3+O2
| ||||
| B、碱式硫酸铁因能水解产生Fe(OH)3胶体,故可用作净水剂 | ||||
| C、为检验暴露在空气中的(NH4)2Fe(SO4)2是否已被氧化,可选用KSCN溶液 | ||||
| D、常温下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的大 |
对于平衡体系mA(g)+nB(g)
pC(g)+qD(g)△H<0.下列结论中错误的是( )
| 催化剂 |
| △ |
| A、若温度不变,将容器的体积缩小到原来的一半,达到新平衡时A的浓度为原来的2.2倍,则m+n<p+q |
| B、若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n |
| C、若m+n=p+q,则向含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a mol |
| D、保持其它条件不变,升高温度,平衡向正反应方向移动 |
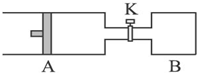 如图所示向A中充入2mol X、2mol Y,向B中充入1mol X、1mol Y,起始时,V(A)=V(B)=a L.在相同温度和有催化剂存在下,两容器中各自发生下述反应:X(g)+Y(g)?2Z(g)+2W(g);△H<0.达到平衡时,V(A)=1.2a L.
如图所示向A中充入2mol X、2mol Y,向B中充入1mol X、1mol Y,起始时,V(A)=V(B)=a L.在相同温度和有催化剂存在下,两容器中各自发生下述反应:X(g)+Y(g)?2Z(g)+2W(g);△H<0.达到平衡时,V(A)=1.2a L.