��Ŀ����
��15�֣�
1-1 2011���ǹ��ʻ�ѧ�꣬�Ǿ�����˻��ŵ������ѧ��100���ꡣ������˷��ֵ����ֻ�ѧԪ�ص�Ԫ�ط��ź��������Ʒֱ��� �� ��
1-2 ��TiOSO4ˮ��Һ�м���п������Ӧ����Һ��Ϊ��ɫ������ҹ�еμ�������CuCl2ˮ��Һ��������ɫ���������ɰ�ɫ���������ӷ���ʽ�� �������μ�CuCl2ˮ��Һ����ɫ������ʧ�������ӷ���ʽ�� ��
1-3 20����60���άҲ�ɴ�ѧV.Gutmann�о�С�鱨������ԭ�ӷ���A����SF4��NH3��Ӧ�ϳɣ�A��AgF2�����õ��е�ΪΪ27�����Ԫ������B��A��B�����е�����ԭ����ͬ�ֶ�λԭ�ӵĺ˼�༸����ȣ�B������һ���������3�����档����A��B�Ľṹʽ����ȷʾ���������ؼ�������ֽ���ϵļ���Ш�μ���ʾ���Ǽ��ϵ��Ӳ��ر������
1-4 ����Al2(n-C4H9)4H2��Mg[Al(CH3)4]2�Ľṹ��ʽ��
1-5 ��֪EӨ(FeO42��/Fe3+) = 2.20 V��EӨ(FeO42��/Fe(OH)3) = 0.72 V��
�� д�����������Ȼ�����Ӧ�γɸ�����������ӷ���ʽ�� ��
�� д���������������ˮ��Һ�зֽ�����ӷ���ʽ�� ��
�� �ø��������þ����ɼ��Ե�أ�д���õ�صĵ缫��Ӧ ��
��15�֣�
1-1 Ra �� Po ��
1-2 Ti3+ + Cu2+ + Cl�� + H2O = TiO2+ + CuCl��+2H+ CuCl + Cl�� = CuCl2��
1-3 
1-4 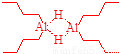
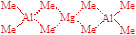
1-5 �� 2Fe3+ + 3Cl2 + 16OH�� = 2FeO42�� + 6Cl�� + 8H2O
�� 4FeO42�� + 20H+ = 4Fe3+ + 3O2 + 10H2O
�� ������FeO42�� + 4H2O + 3e�� = Fe(OH)3 + 5OH��
������Mg + 2OH�� - 2e�� = Mg(OH)2
��������Zn��ǿ��ԭ������TiO2+��ԭ���ͣ�+3����̬�����ͼ�̬Ti�����Ի�ԭ�ԣ���Cu2+��ԭ���Ӷ�����CuCl������

 ��У����ϵ�д�
��У����ϵ�д�