题目内容
16.以Al(OH)3、H2SO4、工业(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如图: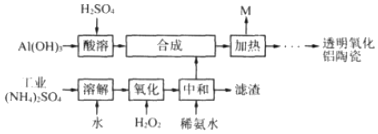
回答下列问题:
(1)写H2O2的作用是氧化亚铁离子为铁离子并写出该步骤中发生的主要反应的离子方程式2Fe2++H2O2+2H+═2Fe3++2H2O;
(2)如何检验中和反应后滤渣中阳离子已完全除尽?取少量中和后的溶液,滴加KSCN溶液,若溶液不变红,则已完全除去;若溶液变红,则未除尽;
(3)写出工业制备金属铝的化学方程式2Al2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑.
分析 Al(OH)3、H2SO4发生反应为2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O;
工业(NH4)2SO4(含FeSO4)溶于水,然后向溶液中加入双氧水,双氧水具有氧化性、硫酸亚铁具有还原性,二者发生氧化还原反应生成铁离子和水,离子方程式为2Fe2++H2O2+2H+═2Fe3++2H2O,将得到的溶液中加入氨水,调节溶液的pH,使铁离子转化为Fe(OH)3沉淀,然后过滤得到滤渣;将滤液加入硫酸铝溶液中,通过分离得到固体NH4Al(SO4)2•12H2O,加热固体NH4Al(SO4)2•12H2O,该物质分解生成M和含铝物质,
(1)双氧水和亚铁离子发生氧化还原反应生成铁离子和水;
(2)中和液中的杂质离子是铁离子,铁离子用KSCN溶液检验;
(3)工业上是电解熔融氧化铝制备金属铝;
解答 解:Al(OH)3、H2SO4发生反应为2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O;
工业(NH4)2SO4(含FeSO4)溶于水,然后向溶液中加入双氧水,双氧水具有氧化性、硫酸亚铁具有还原性,二者发生氧化还原反应生成铁离子和水,离子方程式为2Fe2++H2O2+2H+═2Fe3++2H2O,将得到的溶液中加入氨水,调节溶液的pH,使铁离子转化为Fe(OH)3沉淀,然后过滤得到滤渣;将滤液加入硫酸铝溶液中,通过分离得到固体NH4Al(SO4)2•12H2O,加热固体NH4Al(SO4)2•12H2O,该物质分解生成M和含铝物质,
(1)双氧水和亚铁离子发生氧化还原反应生成铁离子和水,过氧化氢作用是氧化亚铁离子生成铁离子,便于除去,离子反应方程式为2Fe2++H2O2+2H+═2Fe3++2H2O,
故答案为:氧化亚铁离子为铁离子,2Fe2++H2O2+2H+═2Fe3++2H2O;
(2)中和液中的杂质离子是铁离子,铁离子用KSCN溶液检验,其检验方法为取少量中和后的溶液,滴加KSCN溶液,若溶液不变红,则已完全除去;若溶液变红,则未除尽,
故答案为:取少量中和后的溶液,滴加KSCN溶液,若溶液不变红,则已完全除去;若溶液变红,则未除尽;
(3)工业制备金属铝的化学方程式为:2Al2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑,
故答案为:2Al2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑;
点评 本题考查物质制备实验方案评价,为高频考点,侧重考查学生分析、推断、计算能力,明确流程图中发生的反应及基本操作是解本题关键,题目难度中等.

| A. | 含1个双键的环状有机物 | B. | 含2个双键的直链有机物 | ||
| C. | 只含有1个双键的直链有机物 | D. | 含一个三键的直链有机物 |
 为测定某H2C2O4溶液的浓度,取该溶液于锥形瓶中,加入适量稀H2SO4后,用浓度为0.1mol/L KMnO4标准溶液滴定.
为测定某H2C2O4溶液的浓度,取该溶液于锥形瓶中,加入适量稀H2SO4后,用浓度为0.1mol/L KMnO4标准溶液滴定.(提示:滴定原理为:6H++2MnO4-+5H2C2O4═2Mn2++10CO2↑+8H2O)
试回答下列问题:
(1)滴定时,KMnO4溶液应装在酸式(填“酸式”或“碱式”)滴定管中,达到滴定终点时的现象为当滴入最后一滴KMnO4溶液时,溶液由无色变为紫色,且半分钟内不褪色.
(2)如图表示50mL滴定管中液面的位置,此时滴定管中液面的读数为21.40mL.
(3)用0.1mol/L KMnO4标准溶液滴定草酸溶液时,以下操作会使结果偏低的①④(填序号).
①实验结束时俯视刻度线读取滴定终点时KMnO4溶液的体积.
②酸式滴定管未用标准液润洗
③锥形瓶用待测液润洗
④滴加KMnO4溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
(4)该同学一共进行了三次实验,假设每次所取H2C2O4溶液体积均为30.00mL,三次实验结果记录如表:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗KMnO4溶液体积/mL | 30.32 | 25.34 | 25.30 |
| A. | 100mL 1mol/LFeCl3溶液中含有0.1NA个Fe3+ | |
| B. | 1.06g Na2CO3含有的CO32-离子数小于0.01 NA | |
| C. | PH=3的醋酸溶液中,含有的H+数为0.001NA | |
| D. | 2L 0.5mol/L的氨水中,含有NH3•H2O、NH4+、NH3的总数为1 NA |
| A. | 标准状况下,1 mol任何物质体积均为22.4L | |
| B. | CH4的摩尔质量为16g | |
| C. | 3.01×1023个SO2分子的质量为32g | |
| D. | 1 mol H2O的质量为18g/mol |
| A. | 明矾的化学式为Al2(SO4)3•12H2O | |
| B. | 明矾溶于水产生Al(OH)3胶体:Al3++3H2O═Al(OH)3↓+3H+ | |
| C. | AlCl3溶液与浓氨水反应有白色沉淀生成 | |
| D. | Al是重要的金属元素,其对应的氧化物为碱性氧化物 |
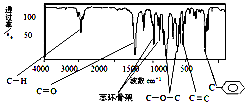
 (不考虑立体异构)
(不考虑立体异构)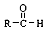 +CH3CHO$\stackrel{稀碱}{→}$
+CH3CHO$\stackrel{稀碱}{→}$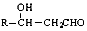 $\stackrel{-H_{2}O}{→}$RCH=CHCHO
$\stackrel{-H_{2}O}{→}$RCH=CHCHO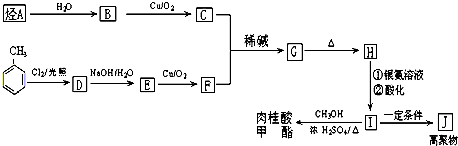

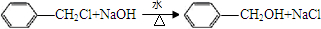
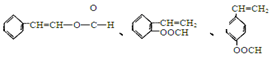
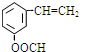 、
、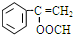 .
.