题目内容
写出下列物质的电子式
H2O KOH
CO2: Na2O2: .
H2O
CO2:
考点:电子式
专题:化学用语专题
分析:(1)水为共价化合物,氧原子最外层8个电子,分子中存在两个氧氢键;
(2)氢氧化钾为离子化合物,电子式需要标出阴阳离子所带电荷;
(3)二氧化碳中存在两个碳氧键,C、O原子最外层都达到最外层8个电子;
(4)过氧化钠为离子化合物,电子式中需要标出阴阳离子所带电荷,注意过氧根离子的表示方法.
(2)氢氧化钾为离子化合物,电子式需要标出阴阳离子所带电荷;
(3)二氧化碳中存在两个碳氧键,C、O原子最外层都达到最外层8个电子;
(4)过氧化钠为离子化合物,电子式中需要标出阴阳离子所带电荷,注意过氧根离子的表示方法.
解答:
解:(1)水中存在两个氧氢键,氧原子最外层达到8电子稳定结构,水的电子式为: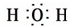 ,
,
故答案为: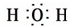 ;
;
(2)氢氧化钾中存在钾离子和氢氧根离子,氢氧化钾的电子式为: ,
,
故答案为: ;
;
(3)二氧化碳中存在两对碳氧共用电子对,二氧化碳的电子式为: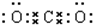 ,
,
故答案为: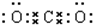 ;
;
(4)Na2O2是离子化合物,由Na+离子和O2-离子构成,Na2O2的电子式为 ,
,
故答案为: .
.
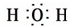 ,
,故答案为:
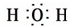 ;
;(2)氢氧化钾中存在钾离子和氢氧根离子,氢氧化钾的电子式为:
 ,
,故答案为:
 ;
;(3)二氧化碳中存在两对碳氧共用电子对,二氧化碳的电子式为:
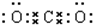 ,
,故答案为:
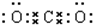 ;
;(4)Na2O2是离子化合物,由Na+离子和O2-离子构成,Na2O2的电子式为
 ,
,故答案为:
 .
.
点评:本题考查了电子式的书写,题目难度中等,注意掌握电子式的概念及表示方法,明确离子化合物与共价化合物的电子式的表示方法及区别.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列说法中错误的是( )
| A、镁的金属性比钠强 |
| B、溴的非金属性比氯强 |
| C、硝酸的酸性比磷酸强 |
| D、水的热稳定性比氨气强 |
用NA表示阿佛加德罗常数,下列叙述正确的是( )
| A、常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA |
| B、通常情况5.6升氢气含0.5NA个原子 |
| C、1L1mol?L-1的NaClO溶液中含有ClO-的数目为NA |
| D、标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA |
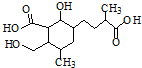 (1)书写化学方程式:①苯乙烯加聚反应;②丙烯与溴的加成反应
(1)书写化学方程式:①苯乙烯加聚反应;②丙烯与溴的加成反应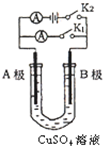 如图所示,U形管内盛有100mL的CuSO4溶液,按要求回答下列问题:
如图所示,U形管内盛有100mL的CuSO4溶液,按要求回答下列问题: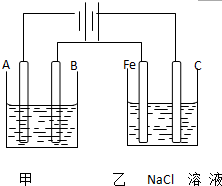 如图为相互串联的甲乙两个电解池,请回答:
如图为相互串联的甲乙两个电解池,请回答: