题目内容
16.由N2O和NO反应生成N2和NO2的能量变化如图所示.下列说法错误的是( )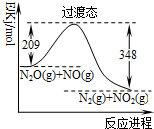
| A. | 使用催化剂可以降低过渡态的能量 | |
| B. | 反应物能量之和大于生成物能量之和 | |
| C. | N2O(g)+NO(g)→N2(g)+NO2(g)+139kJ | |
| D. | 反应物的键能总和大于生成物的键能总和 |
分析 A.催化剂可以降低活化能;
B.根据图象来分析;
C.根据图象可知,此反应放热139KJ;
D.△H=反应物的键能总和-生成物的键能总和.
解答 解:A.催化剂可以降低活化能,降低过渡态的能量,故A正确;
B.根据图象可知,此反应的反应物的总能量大于生成物的总能量,故B正确;
C.根据图象可知,此反应放热139KJ,故热化学方程式为:N2(g)+NO2(g)=N2O(g)+NO(g)+139kJ•mol-1,故C正确;
D.△H=反应物的键能总和-生成物的键能总和,N2(g)+NO2(g)=N2O(g)+NO(g)△H=-139kJ•mol-1,故D错误.
故选D.
点评 本题考查了热化学方程式的书写以及反应吸放热的判断,难度不大,注意反应的实质是旧键的断裂和新键的形成.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.25℃和101kPa时,乙烷、乙炔和丙烯组成的混合烃32mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了72mL,原混合烃中乙炔的体积分数为( )
| A. | 12.5% | B. | 25% | C. | 50% | D. | 75% |
7.下列元素在自然界有以游离态存在的是( )
| A. | S | B. | Na | C. | Si | D. | Cl |
4.晶体从溶液中析出的过程称为结晶,结晶的方法有蒸发溶剂、冷却热饱和溶液等.
(1)已知某盐在不同温度下的溶解度(见下表)
若把质量分数为22%的该盐溶液由60℃逐渐冷却,则开始析出晶体的温度应在D(填字母)
A.0℃~10℃B.10℃~20℃C.20℃~30℃D.30℃~40℃
(2)t℃时,CuSO4在水中溶解度为25g,将32g CuSO4白色粉末加入到mg水中,形成饱和CuSO4溶液,并有CuSO4•5H2O晶体析出,则m的取值范围是18<m<128.
(3)向50mL 4mol/L的NaOH溶液中通入一定量H2S后,将得到的溶液小心蒸干,称得无水物7.97g.请通过计算确定该无水物的成分.
(4)下面是四种盐在不同温度下的溶解度(克/100克水)
(计算时假定:①盐类共存时不影响各自的溶解度;②过滤晶体时,溶剂损耗忽略不计.)
取23.4g NaCl和40.4g KNO3,加70.0g H2O,加热溶解.在100℃时蒸发掉50.0g H2O,维持该温度,过滤出晶体,计算所得晶体质量m1的值.将滤液冷却至10℃,待充分结晶后,过滤,计算所得晶体的质量m2的值.
(1)已知某盐在不同温度下的溶解度(见下表)
| T/℃ | 0 | 10 | 20 | 30 | 40 |
| S(g/100g水) | 11.5 | 15.1 | 19.4 | 24.4 | 37.6 |
A.0℃~10℃B.10℃~20℃C.20℃~30℃D.30℃~40℃
(2)t℃时,CuSO4在水中溶解度为25g,将32g CuSO4白色粉末加入到mg水中,形成饱和CuSO4溶液,并有CuSO4•5H2O晶体析出,则m的取值范围是18<m<128.
(3)向50mL 4mol/L的NaOH溶液中通入一定量H2S后,将得到的溶液小心蒸干,称得无水物7.97g.请通过计算确定该无水物的成分.
(4)下面是四种盐在不同温度下的溶解度(克/100克水)
| NaNO3 | KNO3 | NaCl | KCl | |
| 10℃ | 80.5 | 20.9 | 35.7 | 31.0 |
| 100℃ | 175 | 246 | 39.1 | 56.6 |
取23.4g NaCl和40.4g KNO3,加70.0g H2O,加热溶解.在100℃时蒸发掉50.0g H2O,维持该温度,过滤出晶体,计算所得晶体质量m1的值.将滤液冷却至10℃,待充分结晶后,过滤,计算所得晶体的质量m2的值.
1.下列卤代烃不能够由烃经加成反应制得的是( )
| A. | 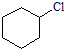 | B. | 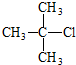 | C. | 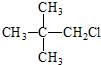 | D. | 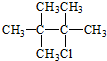 |
8.硝酸与金属反应时,浓度越稀还原产物价态越低.现用一定量的铝粉与镁粉组成的混合物与100mL硝酸钾溶液与硫酸组成的混合溶液充分反应,反应过程中无任何气体放出,向反应后的溶液中逐滴加入4.00mol/L的NaOH溶液,加入的溶液体积与产生的沉淀质量的关系如图所示.下列结论正确的是( )
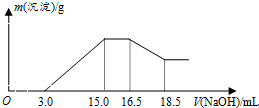

| A. | 铝与混合溶液反应的离子方程式为8Al+30H++3NO3-→8Al3++3NH4++9H2O | |
| B. | 参加反应硝酸根离子物质的量为0.06mol | |
| C. | 参加反应的铝与镁的质量之比为4:3 | |
| D. | 混合液中硫酸的物质的量的浓度为0.36mol/L |
5.下列说法中不正确的是( )
| A. | 正戊烷、新戊烷、异戊烷互为同分异构体 | |
| B. | 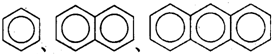 互为同系物 互为同系物 | |
| C. | 四氯乙烯分子中所有原子都处于同一平面 | |
| D. | 扁桃酸(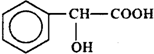 )属于甲酸酯且有羟基直接连在苯环上的同分异构体共有13种 )属于甲酸酯且有羟基直接连在苯环上的同分异构体共有13种 |
6.下列设计的实验方案能达到实验目的是( )
| A. | 检验蔗糖是否水解:蔗糖溶液在稀硫酸存在下水浴加热一段时间后,再与银氨溶液混合加热,观察现象 | |
| B. | 检验溶液中是否含有NH4+:取少量待检验溶液,向其中加入浓NaOH溶液加热,再用湿润的红色石蕊试纸放置试管口,观察现象 | |
| C. | 提纯含有少量苯酚的苯:向含有少量苯酚的苯加入过量浓溴水,振荡后静置过滤,除去三溴苯酚沉淀 | |
| D. | 探究化学反应的限度:取5mL0.1mol/LKI溶液,滴加0.1mol/LFeCl3溶液5~6滴,充分反应,可根据溶液中即含I2又含I-的实验事实判断该反应是可逆反应 |
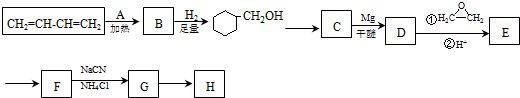
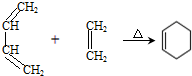

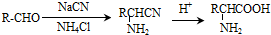
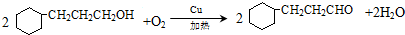 .
.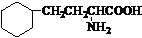 .写出满足下列条件的苯丙氨酸同分异构体的结构简式
.写出满足下列条件的苯丙氨酸同分异构体的结构简式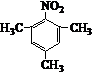 、
、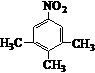 .
.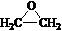 )制备1,4-戊二烯的合成路线(无机试剂任选).
)制备1,4-戊二烯的合成路线(无机试剂任选).