题目内容
甲乙两位同学分别用不同的方法配制100mL 3.6mol/L的稀硫酸.
(1)若采用18mol/L的浓硫酸配制溶液,需要用到浓硫酸的体积为 .
(2)甲学生:量取浓硫酸,小心地倒入盛有少量水的烧杯中,搅拌均匀,待冷却至室温后转移到100mL 容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀.
①将溶液转移到容量瓶中的正确操作是 .
②洗涤操作中,将洗涤烧杯后的洗液也注入容量瓶,其目的是 .
③定容的正确操作是 .
④用胶头滴管往容量瓶中加水时,不小心液面超过了刻度,处理的方法是 (填序号).
A.吸出多余液体,使凹液面与刻度线相切
B.小心加热容量瓶,经蒸发后,使凹液面与刻度线相切
C.经计算加入一定量的浓盐酸
D.重新配制
(3)乙学生:用100mL 量筒量取浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100mL 刻度线,再搅拌均匀.你认为此法是否正确?若不正确,指出其中错误之处 .
(4)下列操作对所得溶液浓度有何影响,在横线上填写:偏高.偏低或无影响
1)烧杯.玻璃棒没洗涤: ;
2)转移时不慎将溶液洒在容量瓶外: ;
3)所用容量瓶的内壁残留有少量蒸馏水: ;
4)定容时俯视容量瓶刻度线: .
(1)若采用18mol/L的浓硫酸配制溶液,需要用到浓硫酸的体积为
(2)甲学生:量取浓硫酸,小心地倒入盛有少量水的烧杯中,搅拌均匀,待冷却至室温后转移到100mL 容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀.
①将溶液转移到容量瓶中的正确操作是
②洗涤操作中,将洗涤烧杯后的洗液也注入容量瓶,其目的是
③定容的正确操作是
④用胶头滴管往容量瓶中加水时,不小心液面超过了刻度,处理的方法是
A.吸出多余液体,使凹液面与刻度线相切
B.小心加热容量瓶,经蒸发后,使凹液面与刻度线相切
C.经计算加入一定量的浓盐酸
D.重新配制
(3)乙学生:用100mL 量筒量取浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100mL 刻度线,再搅拌均匀.你认为此法是否正确?若不正确,指出其中错误之处
(4)下列操作对所得溶液浓度有何影响,在横线上填写:偏高.偏低或无影响
1)烧杯.玻璃棒没洗涤:
2)转移时不慎将溶液洒在容量瓶外:
3)所用容量瓶的内壁残留有少量蒸馏水:
4)定容时俯视容量瓶刻度线:
考点:配制一定物质的量浓度的溶液
专题:
分析:(1)根据浓溶液稀释进行计算用到浓硫酸的体积;
(2)①需要使用玻璃棒引流;
②根据玻璃棒内和烧杯上都沾有一定量溶质分析;
③根据配制一定物质的量浓度溶液的正确定容操作完成;
④不小心液面超过了刻度,配制失败,需要重新配制;
(3)根据浓硫酸的稀释正确操作进行分析;
(4)根据C=
判断.
1)没有洗涤烧杯和玻璃棒,导致溶质物质的量减小;
2)将溶液洒在容量瓶外,导致溶质的物质的量减小;
3)容量瓶内有蒸馏水,不影响配制结果;
4)定容时,俯视容量瓶刻度线,则所配溶液的体积偏小,
(2)①需要使用玻璃棒引流;
②根据玻璃棒内和烧杯上都沾有一定量溶质分析;
③根据配制一定物质的量浓度溶液的正确定容操作完成;
④不小心液面超过了刻度,配制失败,需要重新配制;
(3)根据浓硫酸的稀释正确操作进行分析;
(4)根据C=
| n |
| V |
1)没有洗涤烧杯和玻璃棒,导致溶质物质的量减小;
2)将溶液洒在容量瓶外,导致溶质的物质的量减小;
3)容量瓶内有蒸馏水,不影响配制结果;
4)定容时,俯视容量瓶刻度线,则所配溶液的体积偏小,
解答:
解:(1)配制100mL 3.6mol/L稀硫酸溶液,需要硫酸的物质的量为:3.6mol/L×0.1L=0.36mol,需要浓硫酸的体积为:
=0.020L=20.0mL,
故答案为:20.0mL;
(2)①转移溶液使用玻璃棒,要沿着玻璃棒转移,操作方法为:将玻璃棒插入容量瓶刻度线以下,使溶液沿玻璃棒慢慢地流入容量瓶中,
故答案为:将玻璃棒插入容量瓶刻度线以下,使溶液沿玻璃棒慢慢地流入容量瓶中;
②为了减小误差,配制溶液时必须洗涤烧杯和玻璃棒,以便将溶质完全转移到容量瓶中,
故答案为:使溶质完全转移到容量瓶中;
③转移完洗涤烧杯和玻璃棒的溶液后,开始加入蒸馏水定容,方法为:加水至离刻度线1~2cm时,改用胶头滴管滴加水至液面与刻度线相切,
故答案为:加水至离刻度线1~2cm时,改用胶头滴管滴加水至液面与刻度线相切;
④用胶头滴管往容量瓶中加水时,不小心液面超过了刻度,此次配制操作失败,需要重新配制溶液,
故答案为:D;
(3)用100mL量筒量取浓硫酸,并向其中小心地加入少量水,此操作是错误的,应该是向水中慢慢加入蒸馏水,
故答案为:不能用量筒配制溶液,不能将水加入到浓硫酸中.
(4)1)烧杯、玻璃棒没洗涤,会导致配制的溶液中溶质的物质的量减小,配制溶液的浓度偏低,
故答案为:偏低;
2)转移时不慎将溶液洒在容量瓶外,导致配制的溶液中,溶质的物质的量减少,溶液浓度偏低,
故答案为:偏低;
3)所用容量瓶的内壁残留有少量蒸馏水,不影响配制结果,
故答案为:无影响;
4)定容时,俯视容量瓶刻度线,则所配溶液的体积偏小,物质的量浓度偏高,故答案为:偏高.
| 0.36mol |
| 18mol/L |
故答案为:20.0mL;
(2)①转移溶液使用玻璃棒,要沿着玻璃棒转移,操作方法为:将玻璃棒插入容量瓶刻度线以下,使溶液沿玻璃棒慢慢地流入容量瓶中,
故答案为:将玻璃棒插入容量瓶刻度线以下,使溶液沿玻璃棒慢慢地流入容量瓶中;
②为了减小误差,配制溶液时必须洗涤烧杯和玻璃棒,以便将溶质完全转移到容量瓶中,
故答案为:使溶质完全转移到容量瓶中;
③转移完洗涤烧杯和玻璃棒的溶液后,开始加入蒸馏水定容,方法为:加水至离刻度线1~2cm时,改用胶头滴管滴加水至液面与刻度线相切,
故答案为:加水至离刻度线1~2cm时,改用胶头滴管滴加水至液面与刻度线相切;
④用胶头滴管往容量瓶中加水时,不小心液面超过了刻度,此次配制操作失败,需要重新配制溶液,
故答案为:D;
(3)用100mL量筒量取浓硫酸,并向其中小心地加入少量水,此操作是错误的,应该是向水中慢慢加入蒸馏水,
故答案为:不能用量筒配制溶液,不能将水加入到浓硫酸中.
(4)1)烧杯、玻璃棒没洗涤,会导致配制的溶液中溶质的物质的量减小,配制溶液的浓度偏低,
故答案为:偏低;
2)转移时不慎将溶液洒在容量瓶外,导致配制的溶液中,溶质的物质的量减少,溶液浓度偏低,
故答案为:偏低;
3)所用容量瓶的内壁残留有少量蒸馏水,不影响配制结果,
故答案为:无影响;
4)定容时,俯视容量瓶刻度线,则所配溶液的体积偏小,物质的量浓度偏高,故答案为:偏高.
点评:本题考查了配制一定物质的量浓度的溶液的方法及误差分析,注重了基础知识的考查,可以根据所学知识完成,本题难度不大.

练习册系列答案
相关题目
下列实验操作正确的是( )
| A、可用托盘天平和称量纸称取10.2g NaOH |
| B、某实验需要900ml 0.1mol/L的硫酸铜溶液,则配制该溶液需称取22.5g胆矾晶体 |
| C、用10 mL量筒量取5.2 mL硫酸,仰视时实际量得的液体体积大于5.2 mL |
| D、焰色反应实验中,连续做两个样品时,应将铂丝用硫酸洗净并灼烧到无特殊焰色 |
下列能达到实验目的是( )
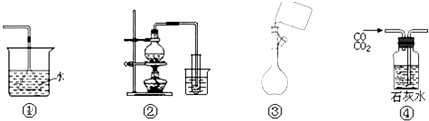

| A、①吸收氨气制氨水 |
| B、②制取少量蒸馏水 |
| C、③向容量瓶中转移溶液 |
| D、④除去CO中的杂质气体CO2 |
下列除去杂质的方法中错误的是( )
| 物质 | 杂质 | 除杂质的方法 | |
| A | CaCl2溶液 | HCl | 过量CaCO3、过滤 |
| B | KNO3溶液 | AgNO3 | 过量NaCl溶液、过滤 |
| C | FeCl2溶液 | CuCl2 | 过量铁粉、过滤 |
| D | CO2 | H2O | 通过盛浓硫酸的洗气瓶 |
| A、A | B、B | C、C | D、D |
可以用分液漏斗分离的一组液体混合物是( )
| A、溴和四氯化碳 |
| B、苯和溴苯 |
| C、乙醇和乙酸 |
| D、水和四氯化碳 |
在4NH3+5O2?4NO+6H2O反应中,表示该反应速率最快的是( )
| A、υ(NH3)=0.8mol/(L?s) |
| B、υ(O2)=1.0mol/(L?s) |
| C、υ(NO)=1.0mol/(L?s) |
| D、υ(H2O)=1.8mol/(L?s) |