题目内容
下列离子方程式书写正确的是( )。
A.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O
B.将少量SO2通入苯酚钠溶液中:2C6H5O-+SO2+H2O=2C6H5OH+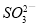
C.用硫氰化钾溶液可以检验溶液中的Fe3+:Fe3++3SCN-=Fe(SCN)3↓
D.向碘化亚铁溶液中通入过量的氯气:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
B
【解析】
试题分析:A、用盐酸酸化的溶液中含有Cl-,高锰酸钾先与氯离子也发生氧化还原反应,错误;B、少量的二氧化硫与苯酚钠溶液反应生成苯酚与亚硫酸根离子,正确;C、Fe(SCN)3是络合物,不是沉淀,错误;D、过量的氯气将亚铁离子、碘离子全部氧化,所以离子方程式中的亚铁离子与碘离子的物质的量之比应是1:2,不是1:1,错误,答案选B。
考点:考查离子方程式的书写

 阅读快车系列答案
阅读快车系列答案碳及其化合物有广泛应用。
(1)工业冶炼铝,以石墨为阳极。阳极反应式为 ,可能发生副反应有 。
(2)一氧化碳和空气在酸性介质中构成燃料电池,负极反应式为 。
(3)向75 mL 4 mol?L-1KOH溶液中缓慢通入4480 mL CO2气体(标准状况)恰好完全被吸收。①写出该反应的离子方程式: 。(只用一个离子方程式表示)
②该吸收溶液中离子浓度大小排序为 。
(4)已知:① 2H2(g)+O2(g)=2H2O(l) △H1=—571.6kJ?mol-1
② 2CO(g)+O2(g)=2CO2(g) △H2 = —566.0kJ?mol-1
③ CO(g)+2H2(g) CH3OH(g) △H3 = —90.8kJ?mol-1
CH3OH(g) △H3 = —90.8kJ?mol-1
计算甲醇蒸气的燃烧热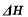 = 。
= 。
(5)某温度下,发生可逆反应:CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g) 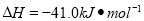
①向某容器中充入1.0 molH2和1.0 molCO2(g),在一定条件下发生上述反应。混合气体中CO的物质的量与时间关系如下列所示:
| 0 | 5 min | 10 min | 15 min | 20 min | 25 min |
I(800℃) | 1.0 | 0.80 | 0.70 | 0.65 | 0.50 | 0.50 |
II(800℃) | 1.0 | 0.7 | 0.60 | 0.50 | 0.50 | 0.50 |
相对实验I,实验II可能改变的条件可能是 ,该温度下,平衡常数= 。
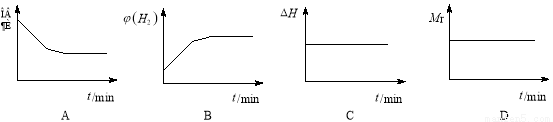
②若开始向绝热容器中投入一定量二氧化碳、氢气在一定条件下发生上述可逆反应。
下列图像正确且说明可逆反应达到平衡状态的是 。(填序号)
 2Z(g),有关下列图像的说法正确的是
2Z(g),有关下列图像的说法正确的是
 的值增大
的值增大