题目内容
取7.8g镁铝合金投入足量盐酸中,充分反应后,测得生成氢气0.4mol,请计算该合金中镁= mol.
考点:有关混合物反应的计算
专题:计算题
分析:令Mg、Al物质的量分别为xmol、ymol,根据二者质量及电子转移守恒列方程计算解答.
解答:
解:令Mg、Al物质的量分别为xmol、ymol,根据二者质量及电子转移守恒,则:
解得x=0.1 y=0.2
故答案为:0.1.
|
解得x=0.1 y=0.2
故答案为:0.1.
点评:本题考查化学方程式有关计算,比较基础,侧重对基础知识的巩固,注意利用电子转移守恒.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列与“低碳经济”不相符的是( )
| A、广泛使用风力发电 |
| B、大力开发化石能源 |
| C、照明大力提倡使用节能灯 |
| D、发展循环经济 |
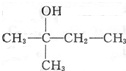 (2)
(2)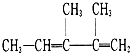 (3)3,4-二甲基己烷 (4)苯乙烯.
(3)3,4-二甲基己烷 (4)苯乙烯.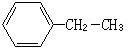
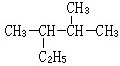
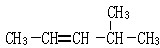
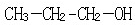 ;2-丙醇:
;2-丙醇: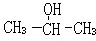 .
.