题目内容
我国规定饮用水质量标准必须符合下列要求
以下是源水处理成自来水的工艺流程示意图:源水→曝气池 一级沉降池
二级沉降池
过滤池→自来水
(1)FeSO4?7H2O是常用的凝聚剂,它在水中最终生成
(2)气体A的作用是 .这种作用是基于气体A和水反应的产物具有 性.
(3)下列物质中 可以作为气体A的代用品(填写编号).①Ca(ClO)2 ②NH3(液) ③K2FeO4 ④SO2.
| pH | 6.5~8.5 |
| Ca2+、Mg2+总浓度 | <0.0045mol?L-1 |
| 细菌总数 | <100个/mL |
| 加入凝聚剂 |
| 通入气体A |
(1)FeSO4?7H2O是常用的凝聚剂,它在水中最终生成
(2)气体A的作用是
(3)下列物质中
考点:"三废"处理与环境保护
专题:化学应用
分析:(1)硫酸亚铁中的亚铁离子水解生成氢氧化亚铁,在空气中最终被氧化为氢氧化铁;
(2)气体A通常为氯气,氯气与水反应生成盐酸和次氯酸,HClO具有强氧化性,能杀菌消毒;
(3)氯气具有强氧化性,能杀菌消毒,则作为Cl2的替代品的物质需具有强氧化性.
(2)气体A通常为氯气,氯气与水反应生成盐酸和次氯酸,HClO具有强氧化性,能杀菌消毒;
(3)氯气具有强氧化性,能杀菌消毒,则作为Cl2的替代品的物质需具有强氧化性.
解答:
解:(1)FeSO4?7H2O是常用的凝聚剂,亚铁离子在溶液中水解生成氢氧化亚铁,氢氧化亚铁具有较强还原性,容易被空气中的氧气氧化成氢氧化铁,所以最终生成的是胶状Fe(OH)3,
故答案为:胶状Fe(OH)3;
(2)气体A为氯气,氯气与水反应生成HCl和HClO,该反应方程式为:Cl2+H2O═HCl+HClO,生成的HClO具有强氧化性,能杀菌消毒,
故答案为:杀菌消毒,强氧化性;
(3)氯气具有强氧化性,其作用为杀菌消毒,能够作为Cl2的替代品的物质必须具有强氧化性,选项中②NH3(液)、④SO2不具有强氧化性,只有①Ca(ClO)2③K2FeO4 具有强氧化性,
故答案为:①③.
故答案为:胶状Fe(OH)3;
(2)气体A为氯气,氯气与水反应生成HCl和HClO,该反应方程式为:Cl2+H2O═HCl+HClO,生成的HClO具有强氧化性,能杀菌消毒,
故答案为:杀菌消毒,强氧化性;
(3)氯气具有强氧化性,其作用为杀菌消毒,能够作为Cl2的替代品的物质必须具有强氧化性,选项中②NH3(液)、④SO2不具有强氧化性,只有①Ca(ClO)2③K2FeO4 具有强氧化性,
故答案为:①③.
点评:本题考查自来水的净化及氯气的化学性质等知识,题目难度不大,注意掌握水的净化原理、氯气、氯水的化学性质,明确各物质的性质、发生的化学反应是解答本题的关键,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
下列关于平衡常数K的说法中,正确的是( )
①平衡常数K只与反应本身及温度有关
②改变反应物浓度或生成物浓度都会改变平衡常数K
③加入催化剂不改变平衡常数K
④平衡常数K只与温度有关,与反应的本身及浓度、压强无关.
①平衡常数K只与反应本身及温度有关
②改变反应物浓度或生成物浓度都会改变平衡常数K
③加入催化剂不改变平衡常数K
④平衡常数K只与温度有关,与反应的本身及浓度、压强无关.
| A、①② | B、②③ | C、③④ | D、①③ |
氮化钠和氢化钠都是离子化合物,与水反应的化学方程式(未配平)如下:
Na3N+H2O→NaOH+NH3
NaH+H2O→NaOH+H2
有关它们的叙述正确的是( )
Na3N+H2O→NaOH+NH3
NaH+H2O→NaOH+H2
有关它们的叙述正确的是( )
| A、离子半径:N3->Na+>H+ |
| B、与水反应都是氧化还原反应 |
| C、与盐酸反应都只生成一种盐 |
| D、两种化合物中的阴阳离子均具有相同的电子层结构 |
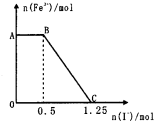 已知酸性高锰酸钾溶液可以将FeS04氧化,方程式为2KMnO4+10FeSO4+8H2SO4═K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示,则下列有关说法不正确的是( )
已知酸性高锰酸钾溶液可以将FeS04氧化,方程式为2KMnO4+10FeSO4+8H2SO4═K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示,则下列有关说法不正确的是( )| A、图中AB段主要是高锰酸钾和碘化钾溶液反应 |
| B、图中BC段发生的反应为2Fe3++2I-═2Fe2++I2 |
| C、向C点以后的溶液中加入少量KSCN溶液,溶液变红色 |
| D、根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.25mol |
下列方程式书写正确的是( )
| A、实验室制取H2:2Fe+6HCl═2FeCl3+3H2↑ | ||||
| B、实验室制取CO2:CaCO3+2HCl═CaCl2+H2O+CO2↑ | ||||
| C、把铜丝伸入硫酸亚铁溶液:Cu+FeSO4═Fe+CuSO4 | ||||
D、甲烷完全燃烧:CH4+O2
|
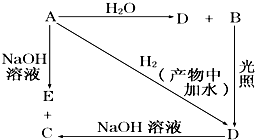 常温下,A是可用来对自来水进行消毒的黄绿色气体单质,A、B、C、D、E都含X元素,其转化关系如图所示.
常温下,A是可用来对自来水进行消毒的黄绿色气体单质,A、B、C、D、E都含X元素,其转化关系如图所示.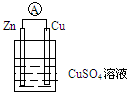 根据如图装置回答:
根据如图装置回答: