题目内容
6.掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置.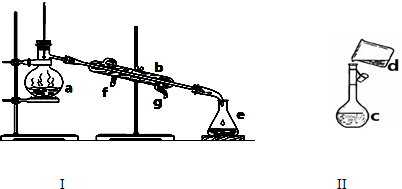
写出下列仪器的名称:
a.蒸馏烧瓶 b.冷凝管 c.容量瓶 e锥形瓶.
分析 由图可知,I为蒸馏装置,分离互溶但沸点不同的液体混合物,Ⅱ为配制一定浓度的溶液,结合图可知仪器的名称,以此来解答.
解答 解:由图可知,I为蒸馏装置,a为蒸馏烧瓶,b为冷凝管,Ⅱ为配制一定浓度的溶液,c为容量瓶,e为锥形瓶,
故答案为:蒸馏烧瓶;冷凝管;容量瓶;锥形瓶.
点评 本题考查混合物分离提纯,为高频考点,把握混合物分离提纯实验、仪器的使用为解答的关键,侧重分析与实验能力的考查,注意分离实验装置,题目难度不大.

练习册系列答案
相关题目
20.实验室配制浓度为2.0mol•L-1 NaOH溶液100mL,下面有关操作及说法正确的是( )
| A. | 配制操作为:称取8 g NaOH固体,放入100 mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀 | |
| B. | 称量 NaOH固体时,应在托盘天平两盘上各放一张大小相同的纸片 | |
| C. | 若所用NaOH固体中有少量Na2O杂质,则造成所配溶液浓度偏高 | |
| D. | 若用10 mol•L-1NaOH溶液来配制,用量筒量取20 mL NaOH浓溶液倒入烧杯后,应该用同一量筒取一定量蒸馏水倒入烧杯中 |
14.一定条件下,溶液的酸碱性对TiO2光催化燃料R降解反应的影响如图所示.下列判断正确的是( )


| A. | 溶液酸性越强,R 的降解速率越小 | |
| B. | R的起始浓度越小,降解速率越大 | |
| C. | 在0~50 min之间,pH=2和PH=7时R的降解百分率相等 | |
| D. | 在20~25 min之间,pH=10 时R的平均降解速率为0.04 mol•L-1•min-1 |
1.中和相同体积、相同pH的硫酸、盐酸和醋酸三种稀溶液,所用相同浓度的NaOH溶液的体积分别为V1、V2、V3,则三者的大小关系为( )
| A. | V3>V2>V1 | B. | V3=V2>V1 | C. | V3>V2=V1 | D. | V1=V2>V3 |
11.相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)?2NH3(g)△H=-92.6kJ/moL.实验测得起始、平衡时得有关数据如表:
下列叙述错误的是( )
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
| A. | 容器①、②中反应的平衡常数相等 | |
| B. | 平衡时,两个容器中NH3的体积分数均为25% | |
| C. | 容器②中达平衡时放出的热量Q=23.15 kJ | |
| D. | 若容器①体积为0.5L,则平衡时放出的热量<23.15kJ |
16.下列说法正确的是( )
| A. | 在常温、常压下,11.2 L N2含有的分子数为0.5NA | |
| B. | 标准状况下,22.4 L H2和O2的混合气体所含分子数为NA | |
| C. | 在标准状况下,1 mol H2和1 mol H2O所占的体积都约为22.4 L | |
| D. | 标准状况下,1 mol CCl4的体积是22.4 L |
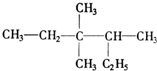 3,3,4-三甲基己烷;
3,3,4-三甲基己烷;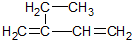 2-乙基-1,3-丁二烯.
2-乙基-1,3-丁二烯.