题目内容
20.常温下,下列各组物质中,Y既能与X反应又能与Z反应的是( )| X | Y | Z | |
| ① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
| ② | KOH溶液 | SiO2 | 氢氟酸 |
| ③ | O2 | N2 | H2 |
| ④ | FeC13溶液 | Cu | 浓硝酸 |
| A. | ①③④ | B. | ①②④ | C. | ②④ | D. | ②③ |
分析 ①氢氧化铝是两性氢氧化物既与酸反应又与碱反应;
②SiO2能与氢氧化钾反应,二氧化硅也能与氢氟酸反应;
③氮气与氧气在放电条件下反应得到NO,氮气与氢气在高温高压、催化剂条件下合成氨气反应;
④Cu与浓硝酸反应生成硝酸铜、二氧化氮与水,与氯化铁溶液反应得到氯化铜、氯化亚铁.
解答 解:①氢氧化铝与氢氧化钠反应生成偏铝酸钠与水,氢氧化铝与稀硫酸反应生成硫酸铝和水,故①符合;
②SiO2能与氢氧化钾反应生成硅酸钾和水,二氧化硅也能与氢氟酸反应生成四氟化硅和水,故②符合;
③氮气与氧气在放电条件下反应得到NO,氮气与氢气在高温高压、催化剂条件下合成氨气反应,常温下氮气不能与氧气、氢气发生反应,故③不符合;
④常温下,Cu与浓硝酸反应生成硝酸铜、二氧化氮与水,与氯化铁溶液反应得到氯化铜、氯化亚铁,故④符合,
故选B.
点评 本题考查元素化合物性质,难度不大,侧重对基础知识的巩固,需要学生熟练掌握元素化合物性质.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
10.某学生以铁丝和Cl2为原料进行下列三个实验.从分类角度下列分析正确的是( )

| A. | 实验①所涉及的物质均为电解质 | |
| B. | 实验②、③得到的分散系中分散质粒子的直径:②>③ | |
| C. | 实验③得到的物质能产生丁达尔现象 | |
| D. | 实验③反应制得的物质为纯净物 |
11.下列说法中,不正确的是( )
| A. | 由于蒸发溶剂而析出晶体后的溶液仍为饱和溶液 | |
| B. | 在饱和溶液中,溶质的溶解速率等于结晶速率 | |
| C. | 任何物质的饱和溶液升高温度时,都变成不饱和溶液 | |
| D. | 溶质刚开始溶解时的溶液为不饱和溶液 |
8.我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务.下列有关海水综合利用的说法不正确的是( )
| A. | 从海水中提炼出的氘(含HDO 0.03‰)进行核聚变,放出巨大的能量以解决能源问题,成为一条新的科学思路,HDO与H2O化学性质相同 | |
| B. | 从海水中提取镁可以采用下列方法:海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{HCl}{→}$MgCl2溶液→MgCl2•6H2O$\stackrel{HCl}{→}$MgCl2 (熔融)$\stackrel{电解}{→}$Mg | |
| C. | 从海水获得的碘,可以跟氧气反应生成多种化合物,其中一种称为碘酸碘,在该化合物中,碘元素呈+3和+5两种价态,这种化合物的化学式是I4O9 | |
| D. | 除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
15. 以下元素均为短周期元素:
以下元素均为短周期元素:
(1)D的最低价含氧酸的电子式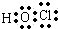 .
.
(2)M的简单气态氢化物与B的单质形成燃料电池(KOH为电解液),写出其负极反应方程式2NH3-6e-+6OH-═N2+6H2O.
(3)仅由A、B、E组成的一种生活中的常用盐,其中A的质量分数为43%,其水溶液与D单质物质的量比1:1反应的离子方程式为CO32-+Cl2+H2O=ClO-+Cl-+HCO-3.
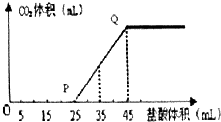
(4)A的最高价氧化物的水化物的溶液中通入一定量CO2得溶液X,X中逐滴加入1mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如图所示:
①X溶液中溶质的化学式NaOH和Na2CO3.
②当加入35mL盐酸时,产生CO2的体积为224mL(标准状况).
 以下元素均为短周期元素:
以下元素均为短周期元素:| 元素代号 | 相关信息 |
| M | 非金属元素,其气态氢化物的水溶液呈碱性 |
| A | A的单质能与冷水剧烈反应,得到强碱性溶液 |
| B | B的原子最外层电子数是其内层电子数的三倍 |
| C | 在第三周期元素中,C的简单离子半径最小 |
| D | A、B、D组成的36电子的化合物X是常用消毒剂的主要成分 |
| E | 所有有机物中都含有E元素 |
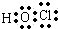 .
.(2)M的简单气态氢化物与B的单质形成燃料电池(KOH为电解液),写出其负极反应方程式2NH3-6e-+6OH-═N2+6H2O.
(3)仅由A、B、E组成的一种生活中的常用盐,其中A的质量分数为43%,其水溶液与D单质物质的量比1:1反应的离子方程式为CO32-+Cl2+H2O=ClO-+Cl-+HCO-3.
(4)A的最高价氧化物的水化物的溶液中通入一定量CO2得溶液X,X中逐滴加入1mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如图所示:
①X溶液中溶质的化学式NaOH和Na2CO3.
②当加入35mL盐酸时,产生CO2的体积为224mL(标准状况).
5.往NH4NO3溶液加入少量Na2O固体,溶液中微粒的数目不变的是( )
| A. | NH4+ | B. | H+ | C. | NO3- | D. | H2O |
12.生物燃料电池是以有机物为燃料,直接或间接利用酶作为催化剂的一类特殊的燃料电池,其能量转化率高,是一种真正意义上的绿色电池,其工作原理如图所示.已知C1极的电极反应为C2H5OH+3H2O-12e-═2CO2+12H+.下列说法中不正确的是( )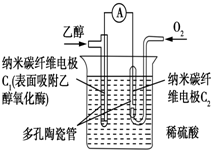

| A. | C1极为电池负极,C2极为电池正极 | |
| B. | 溶液中的H+向C1电极移动 | |
| C. | 该生物燃料电池的总反应方程式为C2H5OH+3O2═2CO2+3H2O | |
| D. | 电流由C2极经外电路流向C1极 |
10.下列说法正确的是( )
| A. | 向10mL浓度为0.1mol•L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中水的电离程度始终增大 | |
| B. | 0.01mol•L-1CH3COOH溶液中水的电离程度小于0.01mol•L-1盐酸中水的电离程度 | |
| C. | 将0.01mol•L-1盐酸与pH=12的氨水等体积混合,所得溶液中由水电离出的c(OH-)<1×10-7mol•L-1 | |
| D. | 将0.01mol•L-1的CH3COOH溶液与pH=12的氨水等体积混合,所得溶液中由水电离出的c(OH-)>1×10-7mol•L-1 |