题目内容
11.在Fe2(SO4)3溶液中滴加无色的KSCN溶液后,有以下可逆反应存在;FeCl3+3KSCN?Fe(SCN)3+3KCl.已知Fe(SCN)3溶液呈红色,则在该平衡体系中加入少量K2SO4晶体后(忽略溶液体积的变化),红色将( )| A. | 不变 | B. | 变浅 | C. | 变深 | D. | 无法确定 |
分析 根据平衡移动原理分析,改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动,而加入少量K2SO4晶体,根据实际参加反应的离子浓度分析,加入少量KCl固体,溶液中Fe3+、SCN-浓度不变.
解答 解:加入少量K2SO4固体,溶液中Fe3+、SCN-浓度不变,K+和SO42-不参加反应,平衡不移动,所以红色不变,故选:A.
点评 本题考查化学平衡的影响因素分析判断,注意建立平衡的微粒分析应用,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
6.下列物质能导电,且属于电解质的是( )
| A. | 铁丝 | B. | 盐酸 | C. | 酒精 | D. | 熔融的NaOH |
19.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 1.0 mol•L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| B. | 甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl- | |
| C. | 无色透明的溶液中:MnO4-、SO42-、Na+、H+ | |
| D. | $\frac{KW}{c(H+)}$=0.1 mol/L的溶液:Na+、K+、SiO32-、NO3- |
6.下列表示对应化学反应的离子方程式正确的是( )
| A. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+=SO2↑+H2O | |
| B. | 漂白粉溶液中通入足量二氧化硫气体:ClO-+SO2+H2O═HClO+HSO${\;}_{3}^{-}$ | |
| C. | NaHCO3溶液中加少量Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O | |
| D. | 向CuSO4溶液中加入Na2O2:2 Na2O2+2Cu2++2H2O═4Na++2Cu(OH)2↓+O2↑ |
16.把质量为a克的铜丝灼烧变黑,立即放入下列物质中,铜丝变红且质量仍为a克的是( )
| A. | 稀硫酸 | B. | 乙醇 | C. | 稀硝酸 | D. | 氢氧化钠溶液 |
3.下列能用离子方程式“H++OH-=H2O”表示的化学反应是( )
| A. | NaOH+HCl═NaCl+H2O | B. | Na2CO3+2HCl═2NaCl+H2O+CO2↑ | ||
| C. | 2KOH+MgCl2═Mg(OH)2↓+2KCl | D. | Zn+H2SO4═ZnSO4+H2↑ |
1.下列反应的离子方程式书写正确的是( )
| A. | 小苏打和盐酸反应:CO32-+2H+═CO2↑+H2O | |
| B. | 氢氧化铝溶于强碱:Al(OH)3+OH-═AlO2-+2H2O | |
| C. | 氢氧化钡溶液与硫酸溶液反应:Ba2++SO42-═BaSO4↓ | |
| D. | 碳酸钙与醋酸反应:CO32-+2H+═H2O+CO2↑ |
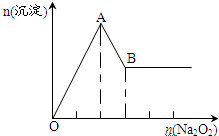 有一透明溶液,可能含有较大量的NH4+、Fe3+、Na+、SO42-、CO32-、H+、Mg2+、Al3+、Cu2+中的某一种或几种,取此溶液做下列试验
有一透明溶液,可能含有较大量的NH4+、Fe3+、Na+、SO42-、CO32-、H+、Mg2+、Al3+、Cu2+中的某一种或几种,取此溶液做下列试验