题目内容
(1)由C、H、O、N、S、P等元素组成的蛋白质,在体内经过消化、吸收,最后氧化成酸: 、H2SO4、H3PO4、尿酸等,这些最终物质是酸性物质,使体液呈弱酸性.因此,这类食物在生理上称为成酸性食物,习惯上称为酸性食物.
(2)某些蔬菜、水果多含K、Na、Ca、Mg等盐类,在人体代谢后生成碱性物质,使体液呈弱碱性,属于 食物.
(3)将100g食品烧成灰分的水溶液用0.1mol/L的酸或碱进行中和,所需酸或碱的体积(单位:mL)定为该食品的碱度或酸度.已知鸡肉的酸度为7.60,则将100g鸡肉烧成灰,溶于水,用0.1mol?L-1的 溶液滴定,该溶液的体积为 mL.
(2)某些蔬菜、水果多含K、Na、Ca、Mg等盐类,在人体代谢后生成碱性物质,使体液呈弱碱性,属于
(3)将100g食品烧成灰分的水溶液用0.1mol/L的酸或碱进行中和,所需酸或碱的体积(单位:mL)定为该食品的碱度或酸度.已知鸡肉的酸度为7.60,则将100g鸡肉烧成灰,溶于水,用0.1mol?L-1的
考点:化学方程式的有关计算,氨基酸、蛋白质的结构和性质特点,人体新陈代谢过程中的生化反应
专题:
分析:(1)蛋白质中还含有C元素,所以生成的酸中应该含有含碳元素的酸;
(2)由物质在人体代谢后生成物的酸碱性将食物分为酸性食物、碱性食物;
(3)鸡肉的酸度为7.60,说明鸡肉烧成灰分的水溶液呈酸性,应该用碱溶液中和,根据酸、碱之间的反应进行计算.
(2)由物质在人体代谢后生成物的酸碱性将食物分为酸性食物、碱性食物;
(3)鸡肉的酸度为7.60,说明鸡肉烧成灰分的水溶液呈酸性,应该用碱溶液中和,根据酸、碱之间的反应进行计算.
解答:
解:(1)蛋白质中还含有C元素,所以生成的酸中应该含有含碳元素的酸,为H2CO3,故答案为:H2CO3;
(2)根据物质在人体代谢后生成物的酸碱性将食物分为酸性食物、碱性食物,某些蔬菜、水果多含K、Na、Ca、Mg等盐类,在人体代谢后生成碱性物质,使体液呈弱碱性,所以这些物质属于碱性食物,故答案为:碱性;
(3)鸡肉的酸度为7.60,说明鸡肉烧成灰分的水溶液呈酸性,应该用碱NaOH溶液中和;根据酸度的概念知,需要酸的体积(mL)就是其酸度,所以鸡肉的酸度为7.60,则将100g鸡肉烧成灰,溶于水,用0.1mol?L-1的NOH溶液滴定,该溶液的体积为7.60,
故答案为:NaOH;7.60.
(2)根据物质在人体代谢后生成物的酸碱性将食物分为酸性食物、碱性食物,某些蔬菜、水果多含K、Na、Ca、Mg等盐类,在人体代谢后生成碱性物质,使体液呈弱碱性,所以这些物质属于碱性食物,故答案为:碱性;
(3)鸡肉的酸度为7.60,说明鸡肉烧成灰分的水溶液呈酸性,应该用碱NaOH溶液中和;根据酸度的概念知,需要酸的体积(mL)就是其酸度,所以鸡肉的酸度为7.60,则将100g鸡肉烧成灰,溶于水,用0.1mol?L-1的NOH溶液滴定,该溶液的体积为7.60,
故答案为:NaOH;7.60.
点评:本题考查方程式的计算、食物酸碱性的判断等知识点,侧重考查化学与生活及学生自学能力,明确食物中成分,合理膳食,营养均衡,题目难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
在强酸性溶液中,下列各组离子能大量共存的是( )
| A、Mg2+、OH-、SO42- |
| B、Ag+、Al3+、Cl- |
| C、Cu2+、Cl-、SO42- |
| D、Fe3+、NH4+、SCN- |
把CO2通入下列饱和溶液中,最终一定会有沉淀的是( )
| A、CaCl2 |
| B、Na2CO3 |
| C、Ca(OH)2 |
| D、NaNO3 |
下列微粒中,与OH-具有相同的质子数和相同的电子数的是( )
| A、F- |
| B、H2O |
| C、NH4+ |
| D、NH3 |
物质的量均为0.4mol的 Na、Mg、Al 分别与150ml 浓度为2mol/L的盐酸反应,相同温度和压强下比较产生H2的体积 ( )
| A、Na产生的多 |
| B、Mg产生的多 |
| C、Al产生的多 |
| D、一样多 |
埋在地下的自来水管,在下列情况下被腐蚀的速度最慢的是( )
| A、在含有铁元素的较多的酸性土壤中 |
| B、在潮湿、疏松的土壤中 |
| C、在自来水的铁管上用导线连接一块锌片后,再埋入不透气的土壤中 |
| D、在自来水的铁管上用导线连接一块铜片后,再埋入潮湿、疏松的土壤中 |
下列说法中,正确的是( )
| A、△H>0表示放热反应,△H<0 表示吸热反应 |
| B、若反应△H>0;△S<0,则反应一定能自发进行 |
| C、1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热 |
| D、热化学方程式中的化学计量数表示物质的量,所以可以是分数 |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ/mol
②CH3OH(g)+
O2(g)=CO2(g)+2H2(g);△H=-192.9kJ/mol
下列说法错误的是( )
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ/mol
②CH3OH(g)+
| 1 |
| 2 |
下列说法错误的是( )
| A、1mol CH3OH(g)完全燃烧放出的热量大于192.9 kJ | ||
B、根据反应①和②推知反应:H2(g)+
| ||
| C、CH3OH转变成H2的过程不一定要吸收能量 | ||
D、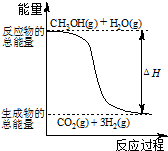 反应①中的能量变化如图所示 |