题目内容
将一小块焦炭和xgO2同时放入装有压力表的密闭容器中,压强为P0,当在一定条件下充分反应后恢复到原温度,压强为P1,且P0<P1<2P0,则加入焦炭的质量m为( )
A、m≤
| ||
B、m≥
| ||
C、m>
| ||
D、m=
|
考点:化学方程式的有关计算
专题:计算题
分析:根据在相同温度和相同体积的条件下,密闭容器中气体分子数与表现出来的压强成正比例关系,可判断反应前后气体的分子数目的改变,据碳在氧气中充分燃烧与不充分燃烧的规律,此时碳应充分燃烧全部生成一氧化碳或二氧化碳,据碳在氧气中完全燃烧的化学方程式,由反应中碳与所消耗氧气的质量关系,判断密闭容器中mg碳和ng氧气的关系.
解答:
解:根据题意,密闭容器中气体分子数与表现出来的压强成正比例关系,由C+O2
CO2与2C+O2
2CO可知,若反应前后分子数目不变,可判断碳在氧气中充分燃烧只生成二氧化碳,若分子数目变大,则只生成一氧化碳或一氧化碳二氧化碳共存,即说明C过量,部分CO2转化为CO,那么O2是完全参与反应的.
假设m1g碳和xg氧气恰好完全反应生成二氧化碳,则
C+O2
CO2
12 32
m1g xg
则m1=
=
剩余碳:(m-
)g,物质的量是(
-
)mol,
由C+CO2
2CO可知每1mol C参与反应气体物质的就会多出1mol,
那么剩余的(
-
)mol C与CO2反应,气体物质的量就会多出(
-
)mol,
此时气体总物质的量应该是
+(
-
)mol=
mol,
密闭容器中气体的物质的量之比等于压强之比,所以
:
=P0:P1,解得m=
如果P0<P1<2P0,是既生成二氧化碳又生成一氧化碳,则m与x应满足的关系是m>
g,
故选C.
| ||
| ||
假设m1g碳和xg氧气恰好完全反应生成二氧化碳,则
C+O2
| ||
12 32
m1g xg
则m1=
| 12x |
| 32 |
| 3x |
| 8 |
| 3x |
| 8 |
| m |
| 12 |
| x |
| 32 |
由C+CO2
| ||
那么剩余的(
| m |
| 12 |
| x |
| 32 |
| m |
| 12 |
| x |
| 32 |
此时气体总物质的量应该是
| x |
| 32 |
| m |
| 12 |
| x |
| 32 |
| m |
| 12 |
密闭容器中气体的物质的量之比等于压强之比,所以
| x |
| 32 |
| m |
| 12 |
| 3xP1 |
| 8P0 |
如果P0<P1<2P0,是既生成二氧化碳又生成一氧化碳,则m与x应满足的关系是m>
| 3xP1 |
| 8P0 |
故选C.
点评:本题考查学生碳和氧气之间的反应知识,注意恒温恒容条件下,密闭容器中气体的物质的量之比等于压强之比,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
一定温度下,Mg(OH)2在下列液体中的溶解度,由大到小的顺序是( )
①50mL蒸馏水;②20mL 0.5mol/L MgCl2溶液;③100mL 0.5mol/L NaOH溶液;④30mL 0.2mol/L NaHSO4溶液;⑤60mL 0.2mol/L NH4Cl溶液.
①50mL蒸馏水;②20mL 0.5mol/L MgCl2溶液;③100mL 0.5mol/L NaOH溶液;④30mL 0.2mol/L NaHSO4溶液;⑤60mL 0.2mol/L NH4Cl溶液.
| A、①②③④⑤ |
| B、④⑤①②③ |
| C、⑤④①②③ |
| D、④⑤①③② |
将a mol FeS与b mol Fe(a>b)的混合物投入到VL c mol/L的硝酸溶液中,固体完全溶解,设还原产物全部为NO气体,且硫元素在溶液中全部以SO42-的形式存在,则反应过程中未被还原的硝酸的物质的量可能为( )
| A、2(a+b) | ||
| B、a+3b | ||
C、cV-
| ||
D、cV-
|
现有久置的氯水、新制的氯水、氯化钠、氢氧化钠四种溶液,可加入一种试剂就能区别它们,则这种试剂是( )
| A、硝酸银溶液 |
| B、酚酞溶液 |
| C、紫色石蕊溶液 |
| D、饱和食盐水 |
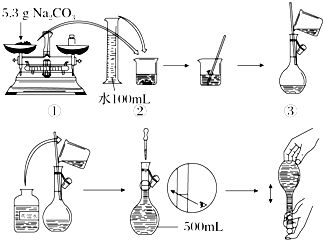 用Na2CO3?10H2O晶体,配制0.2mol?L-1的Na2CO3溶液480mL.
用Na2CO3?10H2O晶体,配制0.2mol?L-1的Na2CO3溶液480mL.