题目内容
6.将等质量的a、b两份锌粉装入试管中,分别加入过量的稀硫酸,同时向装a的试管中加入少量CuSO4溶液.如图表示产生氢气的体积V与时间t的关系,其中正确的是( )| A. | 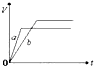 | B. |  | C. | 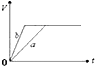 | D. |  |
分析 Zn和硫酸反应,a中加入CuSO4,会置换出金属Cu,形成Zn、Cu、稀硫酸原电池,加速金属Zn和硫酸反应的速率,产生氢气的量取决于和稀硫酸反应的Zn的质量,据此分析解答.
解答 解:Zn和硫酸反应,a中加入CuSO4,会置换出金属Cu,形成Zn、Cu、稀硫酸原电池,加速金属Zn和硫酸反应的速率,所以反应速率a>b;
产生氢气的量取决于和稀硫酸反应的Zn的质量,a中部分Zn和铜离子反应、b中Zn完全和稀硫酸反应,所以生成的氢气:a<b,
故选A.
点评 本题考查了根据图象判断反应速率的大小,难度不大,分析图象时注意图象中坐标的含义、拐点变化趋势,注意原电池能增大化学反应速率,题目难度不大.

练习册系列答案
相关题目
7.向烧杯中加入一定量的蔗糖,加水湿润后,加入浓硫酸搅拌,经过一系列的变化以后形成“黑面包”.在此实验中不能体现出浓硫酸的性质是( )
| A. | 吸水性 | B. | 脱水性 | C. | 强氧化性 | D. | 酸性 |
8.下列各组物质、按单质、电解质、混合物顺序排列的是( )
| A. | 铁、纯碱、冰水混合物 | B. | 氢气、陶瓷、漂白粉 | ||
| C. | 液氧、烧碱、碘酒 | D. | 金刚石、二氧化碳、漂粉精 |
18.NA表示阿伏伽德罗常数,下列判断正确的是( )
| A. | 在18g${\;}_{\;}^{18}$O2中含有NA个氧分子 | |
| B. | 标准状况下,22.4L空气含有NA个单质分子 | |
| C. | 1 molCI2参加反应转移电子数可能为1NA | |
| D. | 含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol•L-1 |
15. 溴乙烷是一种重要的化工合成原料.实验室合成溴乙烷的实验装置如下:实验中可能用到的数据如表:
溴乙烷是一种重要的化工合成原料.实验室合成溴乙烷的实验装置如下:实验中可能用到的数据如表:
①合成反应:在仪器B中加入适量NaBr、浓硫酸和50ml乙醇,安装好仪器,缓缓加热,收集馏出物.
②分离提纯:将馏出物加水后振荡,再加入适量酸除去乙醚,分液,最后得到52mL溴乙烷.
回答下列问题:
(1)仪器B的名称是蒸馏烧瓶,B中发生的主要反应有:NaBr+H2SO4=NaHSO4+HBr,以及HBr+CH3CH2OH$\stackrel{△}{→}$CH3CH2Br+H2O
(2)仪器C为直形冷凝管,冷水进口是b(填“a”或“b”)
(3)仪器D置于盛有冰水混合的烧杯中,目的是冷却溴乙烷
(4)溴乙烷粗产品分离提纯阶段,加水的目的是除去溶解在溴乙烷中乙醇
(5)该实验所得溴乙烷的产率为79%.
 溴乙烷是一种重要的化工合成原料.实验室合成溴乙烷的实验装置如下:实验中可能用到的数据如表:
溴乙烷是一种重要的化工合成原料.实验室合成溴乙烷的实验装置如下:实验中可能用到的数据如表:| 物 质 | 相对分子质量 | 沸点(℃) | 密度(g•cm-3) | 水溶性 |
| CH3CH2OH | 46 | 78.4 | 0.79 | 互溶 |
| CH3CH2Br | 109 | 38.4 | 1.42 | 难溶 |
| CH3CH2OCH2CH3 | 74 | 34.5 | 0.71 | 微溶 |
| CH2=CH2 | 28 | -103.7 | 0.38 | 不溶 |
| 浓硫酸(H2SO4) | 98 | 338.0 | 1.38 | 易溶 |
②分离提纯:将馏出物加水后振荡,再加入适量酸除去乙醚,分液,最后得到52mL溴乙烷.
回答下列问题:
(1)仪器B的名称是蒸馏烧瓶,B中发生的主要反应有:NaBr+H2SO4=NaHSO4+HBr,以及HBr+CH3CH2OH$\stackrel{△}{→}$CH3CH2Br+H2O
(2)仪器C为直形冷凝管,冷水进口是b(填“a”或“b”)
(3)仪器D置于盛有冰水混合的烧杯中,目的是冷却溴乙烷
(4)溴乙烷粗产品分离提纯阶段,加水的目的是除去溶解在溴乙烷中乙醇
(5)该实验所得溴乙烷的产率为79%.
16.25℃时,下列溶液中各离子的浓度关系正确的是( )
| A. | 0.1mol•L-1的CH3COONa溶液中:c(CH3COO-)+c(CH3COOH)>0.1mol•L-1 | |
| B. | 等物质的量浓度的Na2CO3溶液与NaHCO3溶液相比,前者的c(H+)更小 | |
| C. | pH=9.4,浓度均为0.1mol•L-1的HCN与NaCN的混合溶液中:c(Na+)>c(HCN)>c(CN-)>c(OH-) | |
| D. | 将少量AgCl分别加入等体积等物质的量浓度的NaBr溶液与KI溶液中,充分反应后,后者的c(Ag+)更大 |