题目内容
(1)常温下,0.1mol/L的盐酸的pH= ;
(2)常温下,某醋酸溶液的pH=1,其浓度 0.1mol/L(填“>”、“<”或“=”);
(3)用标准盐酸来滴定待测氢氧化钠溶液,选用 (填“甲基橙”或“石蕊”)作指示剂,若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,则滴定结果(氢氧化钠的浓度) (填“偏高”、“偏低”或“无影响”);
(4)向饱和的AgCl溶液中加入NaBr(aq),有淡黄色沉淀生成,说明Ksp(AgCl) Ksp(AgBr)(填“>”、“<”或“=”).
(2)常温下,某醋酸溶液的pH=1,其浓度
(3)用标准盐酸来滴定待测氢氧化钠溶液,选用
(4)向饱和的AgCl溶液中加入NaBr(aq),有淡黄色沉淀生成,说明Ksp(AgCl)
考点:pH的简单计算,难溶电解质的溶解平衡及沉淀转化的本质
专题:
分析:(1)一元强酸溶液中氢离子浓度等于酸浓度,根据PH=-lgc(H+)计算;
(2)醋酸为弱电解质,在溶液中部分电离;
(3)氢氧化钠与盐酸恰好反应时溶液呈中性,可用甲基橙做指示剂;根据操作对c(待测)=
产生的影响分析误差;
(4)化学式相似的物质的溶度积常数越小,则物质越难溶,根据沉淀的转化的角度分析;
(2)醋酸为弱电解质,在溶液中部分电离;
(3)氢氧化钠与盐酸恰好反应时溶液呈中性,可用甲基橙做指示剂;根据操作对c(待测)=
| c(标准)×V(标准) |
| V(待测) |
(4)化学式相似的物质的溶度积常数越小,则物质越难溶,根据沉淀的转化的角度分析;
解答:
解:(1)盐酸为强酸,0.1mol/L的盐酸,PH=-lgc(H+)=-lg0.1=1,
故答案为:1;
(2)常温下,某醋酸溶液的pH=1,根据PH=-lgc(H+),c(H+)=0.1mol/L,醋酸为弱电解质,在溶液中部分电离,其浓度大于0.1mol/L,
故答案为:>;
(3)甲基橙的变色范围是3.1-4.4,且变色现象较明显,所以该中和滴定可以用甲基橙作指示剂,若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,导致待测液的物质的量增加,消耗的标准液体积增大,结果偏高,
故答案为:甲基橙;偏高;
(4)在AgCl饱和溶液中加入足量浓NaBr溶液可生成AgBr沉淀,说明AgBr比AgCl更难溶,说明Ksp(AgCl)>Ksp(AgBr),
故答案为:>;
故答案为:1;
(2)常温下,某醋酸溶液的pH=1,根据PH=-lgc(H+),c(H+)=0.1mol/L,醋酸为弱电解质,在溶液中部分电离,其浓度大于0.1mol/L,
故答案为:>;
(3)甲基橙的变色范围是3.1-4.4,且变色现象较明显,所以该中和滴定可以用甲基橙作指示剂,若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,导致待测液的物质的量增加,消耗的标准液体积增大,结果偏高,
故答案为:甲基橙;偏高;
(4)在AgCl饱和溶液中加入足量浓NaBr溶液可生成AgBr沉淀,说明AgBr比AgCl更难溶,说明Ksp(AgCl)>Ksp(AgBr),
故答案为:>;
点评:本题考查了PH简单计算,弱电解质的电离、中和滴定操作误差分析,难溶电解质的沉淀转化等知识,题目难度不大,注意化学式相似的物质的溶度积常数越小,则物质越难溶,为高频考点.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
实验是化学研究的基础.下列对实验现象的描述错误的是( )
 |  | 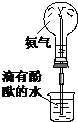 |  |
| ① | ② | ③ | ④ |
| A、实验①中溶液变黄色 |
| B、实验②试管中混合溶液变红色 |
| C、实验③中烧瓶内溶液变红色 |
| D、实验④中出现砖红色沉淀 |
下列关于电解质的说法正确的是( )
| A、不是电解质的物质就是非电解质 |
| B、将纯水加热至较高温度,Kw变大 |
| C、BaSO4不溶于水,其水溶液的导电能力很弱,所以为弱电解质 |
| D、电解质在任何状态下都能导电 |
下列说法正确的是( )
| A、垃圾处理常用的方法是卫生填埋、堆肥和焚烧 |
| B、将垃圾分类并回收是处理的发展方向 |
| C、填埋垃圾不需要治理,只需深埋即可 |
| D、垃圾是污染物,不会产生二次污染 |
照反应Br+H2?HBr+H的能量变化示意图,下列叙述正确的是( )
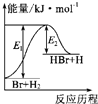

| A、该反应的△H=+(E1-E2)kJ?mol-1 |
| B、加入催化剂,该化学反应的反应热变大 |
| C、反应物的总能量高于生成物的总能量 |
| D、该反应为放热反应 |
根据下列反应,判断氧化性强弱正确的是( )
①2H2S+O2═2S↓+2H2O ②4NaI+O2+2H2O═4NaOH+2I2 ③Na2S+I2═2NaI+S↓
①2H2S+O2═2S↓+2H2O ②4NaI+O2+2H2O═4NaOH+2I2 ③Na2S+I2═2NaI+S↓
| A、O2>I2>S |
| B、O2>S>I2 |
| C、I2>O2>S |
| D、S>I2>O2 |
高铁酸钾(K2FeO4)是一种高效绿色水处理剂,其工业制备的反应原理为:2Fe(OH)3+3KClO+4KOH=2K2FeO4+3KCl+5H2O,下列说法正确的是( )
| A、制高铁酸钾用 KClO做还原剂 |
| B、Fe(OH)3是还原剂 |
| C、高铁酸钾中铁的化合价为+7 |
| D、制备高铁酸钾时1 molFe(OH)3得到3 mol电子 |
 化学兴趣小组设计以下实验方案,测定某已部分变质的小苏打样品中NaHCO3的质量分数.
化学兴趣小组设计以下实验方案,测定某已部分变质的小苏打样品中NaHCO3的质量分数.