题目内容
高考是知识、能力与技巧的较量,在有限的时间内,时间决定成败.大多数考生不是不会做高考题,而是时间不够,尤其是理综考试,很难完成全卷.导致时间紧张的重要原因之一是缺乏解题技巧,因此,在高考冲刺阶段,掌握题型与技巧关系尤为重要.请完成下列计算:
(1)设NA为阿伏加德罗常数,如果ag某气态双原子分子的分子数为p,则b g该气体在标准状况下的体积为 L.
(2)有一瓶14%的KOH溶液,加热蒸发掉100g 水后,变为28%的KOH溶液80mL,该80mL 溶液的物质的量浓度为 mol/L (计算结果精确到小数点后2位)
(3)请根据反应15CuSO4+11P+24H2O═5Cu3P+6H3PO4+15H2SO4,判断1mol CuSO4能氧化P的物质的量 mol.
(4)将a L NH3通过灼热的装有铁触媒的硬质玻璃管后,气体体积变为b L(气体体积均在同温同压下测定),该b L气体中NH3的体积分数是 .
(1)设NA为阿伏加德罗常数,如果ag某气态双原子分子的分子数为p,则b g该气体在标准状况下的体积为
(2)有一瓶14%的KOH溶液,加热蒸发掉100g 水后,变为28%的KOH溶液80mL,该80mL 溶液的物质的量浓度为
(3)请根据反应15CuSO4+11P+24H2O═5Cu3P+6H3PO4+15H2SO4,判断1mol CuSO4能氧化P的物质的量
(4)将a L NH3通过灼热的装有铁触媒的硬质玻璃管后,气体体积变为b L(气体体积均在同温同压下测定),该b L气体中NH3的体积分数是
考点:化学方程式的有关计算,物质的量的相关计算,物质的量浓度的相关计算,氧化还原反应的计算,有关混合物反应的计算
专题:计算题
分析:(1)根据M=
=
计算其摩尔质量,再根据V=
Vm计算气体体积;
(2)根据蒸发过程中溶质的质量不变计算溶质的质量,再根据C=
计算溶质的物质的量浓度;
(3)15CuSO4+11P+24H2O═5Cu3P+6H3PO4+15H2SO4中Cu元素化合价由+2价变为+1价、P元素化合价由0价变为-3价、+5价,根据转移电子守恒计算被氧化的P的物质的量;
(4)氨气在热的铁触媒作用下发生分解反应:2NH3
N2+3H2,气体体积变化(b-a)L,由方程式差量可知,参加反应的氨气为(b-a)L,所以剩余的氨气的体积为(2a-b)L,在根据体积分数定义计算.
| m |
| n |
| m | ||
|
| m |
| M |
(2)根据蒸发过程中溶质的质量不变计算溶质的质量,再根据C=
| ||
| V |
(3)15CuSO4+11P+24H2O═5Cu3P+6H3PO4+15H2SO4中Cu元素化合价由+2价变为+1价、P元素化合价由0价变为-3价、+5价,根据转移电子守恒计算被氧化的P的物质的量;
(4)氨气在热的铁触媒作用下发生分解反应:2NH3
| ||
| △ |
解答:
解:(1)设该气体的摩尔质量为M,M=
=
=
g/mol=
g/mol,则bg该气体在标况下体积=nVm=
Vm=
×22.4L/mol=
L,
故答案为:
;
(2)设原来溶液的质量为xg,蒸发过程中溶质的质量不变,则14%xg=(x-100)g×28%,则x=200,
n(KOH)=
=0.5mol,蒸发掉100g水后溶液的物质的量浓度=
=6.25mol/L,
故答案为:6.25 mol/L;
(3)15CuSO4+11P+24H2O═5Cu3P+6H3PO4+15H2SO4中Cu元素化合价由+2价变为+1价、P元素化合价由0价变为-3价、+5价,1mol CuSO4完全反应转移电子的物质的量为1mol,根据转移电子相等,当有1molCuSO4反应时,被氧化的P的物质的量=
=0.2mol,
故答案为:0.2;
(4)气体体积变化(b-a)L,则:
2NH3
N2+3H2 体积增大△V
2 1 3 1+3-2=2
(b-a)L (b-a)L
所以混合气体中氨气的体积为aL-(b-a)L=(2a-b)L.
所以该b L气体中的NH3体积分数是=
=
,
故答案为:
.
| m |
| n |
| m | ||
|
| a | ||
|
| aNA |
| p |
| m |
| M |
| bg | ||
|
| 22.4pb |
| aNA |
故答案为:
| 22.4pb |
| aNA |
(2)设原来溶液的质量为xg,蒸发过程中溶质的质量不变,则14%xg=(x-100)g×28%,则x=200,
n(KOH)=
| 200g×14% |
| 56g/mol |
| 0.5mol |
| 0.08L |
故答案为:6.25 mol/L;
(3)15CuSO4+11P+24H2O═5Cu3P+6H3PO4+15H2SO4中Cu元素化合价由+2价变为+1价、P元素化合价由0价变为-3价、+5价,1mol CuSO4完全反应转移电子的物质的量为1mol,根据转移电子相等,当有1molCuSO4反应时,被氧化的P的物质的量=
| 1mol |
| 5 |
故答案为:0.2;
(4)气体体积变化(b-a)L,则:
2NH3
| ||
| △ |
2 1 3 1+3-2=2
(b-a)L (b-a)L
所以混合气体中氨气的体积为aL-(b-a)L=(2a-b)L.
所以该b L气体中的NH3体积分数是=
| (2a-b)L |
| bL |
| 2a-b |
| b |
故答案为:
| 2a-b |
| b |
点评:本题考查物质的量的计算,难度不大,注意(3)题中P既被氧化又被还原,注意(4)氨气在试管中发生反应是关键,注意不是氨的催化氧化反应,灵活运用差量法解答(4)题.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
已知标准状况下,5.6L Y气体的质量为16g,则Y气体的摩尔质量是( )
| A、16g |
| B、32g |
| C、64g/mol |
| D、32g/mol |
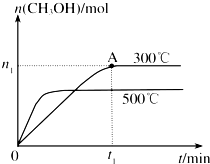 甲醇是一种可再生燃料.在容积为2L的密闭容器中进行反应:CO(g)
甲醇是一种可再生燃料.在容积为2L的密闭容器中进行反应:CO(g)
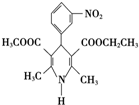 尼群地平片可用于治疗高血压.其药理作用是引起冠状动脉、肾小动脉等全身血管扩张,产生降压作用.它的主要成分的结构简式如下:
尼群地平片可用于治疗高血压.其药理作用是引起冠状动脉、肾小动脉等全身血管扩张,产生降压作用.它的主要成分的结构简式如下: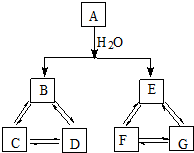 有A、B、C、D、E、F、G七种常见物质,它们满足下图所示转化关系.已知:
有A、B、C、D、E、F、G七种常见物质,它们满足下图所示转化关系.已知: