题目内容
现有一瓶失去标签的纯净的铵盐,为测定其中的含氮量可以采用“甲醛法”,即:4A.17.5% B.17.7% C.21.2% D.35%
D
解析:要符合题意必须满足两个条件:(1)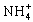 )=0.025mol;(2)纯净铵盐。所以突破此题的关键是推断出满足上述条件的铵盐。推断过程,第一种情况,若酸根离子不含N元素,则铵盐的化学式为(NH4)nR,Rn-为酸根离子,则(NH4)nR中
)=0.025mol;(2)纯净铵盐。所以突破此题的关键是推断出满足上述条件的铵盐。推断过程,第一种情况,若酸根离子不含N元素,则铵盐的化学式为(NH4)nR,Rn-为酸根离子,则(NH4)nR中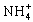 的物质的量为0.025/n,所以(NH4)nR的摩尔质量为2n/0.025(g/mol)=80n(g/mol),当n=1,M=
的物质的量为0.025/n,所以(NH4)nR的摩尔质量为2n/0.025(g/mol)=80n(g/mol),当n=1,M=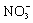 ),因此铵盐为NH4NO3,2gNH4NO3中
),因此铵盐为NH4NO3,2gNH4NO3中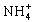 的物质的量为0.025mol,与题意相符,其中的氮的质量分数为35%,总之,铵盐只能是NH4NO3,所以D正确。
的物质的量为0.025mol,与题意相符,其中的氮的质量分数为35%,总之,铵盐只能是NH4NO3,所以D正确。

练习册系列答案
相关题目