题目内容
7.下列说法正确的是( )| A. | 第IA族元素的金属性比第IIA族元素的金属性强 | |
| B. | 原子最外层只有2个电子的元素一定是第ⅡA元素 | |
| C. | 碱金属的熔点和密度都是随着原子序数的增大而增大 | |
| D. | 如果发现了原子序数为117号元素,它应该属于金属元素 |
分析 A.Ca的金属性大于Na;
B.原子最外层只有2个电子的元素还可能为He或某些过渡金属元素;
C.碱金属的熔点随着原子序数的增大而减小;
D.如果发现了原子序数为117号元素,为第七周期第ⅤⅡA元素.
解答 解:A.Ca的金属性大于Na,则同周期第IA族元素的金属性比第IIA族元素的金属性强,故A错误;
B.原子最外层只有2个电子的元素还可能为He或某些过渡金属元素,则不一定为第ⅡA元素,故B错误;
C.碱金属的熔点随着原子序数的增大而减小,而密度随着原子序数的增大而增大,但Na的密度大于K,故C错误;
D.如果发现了原子序数为117号元素,为第七周期第ⅤⅡA元素,由同主族元素性质的递变性可知,应该属于金属元素,故D正确;
故选D.
点评 本题考查元素周期表结构及应用,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,注意碱金属性质,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
17.下列说法中正确的是( )
| A. | HF、HCl、H2S、PH3的稳定性依次增强 | |||||||||||||||
| B. | 按Mg、Si、N、F的顺序,原子半径由小变大 | |||||||||||||||
| C. | 某主族元素的电离能I1~I7数据如表所示(单位:kJ/mol),可推测该元素位于元素周期表第ⅤA族
| |||||||||||||||
| D. | 在①P、S,②Mg、Ca,③Al、Si三组元素中,每组中第一电离能较大的元素的原子序数之和为41 |
2.下列既属于氧化还原反应,又属于吸热反应的是( )
| A. | 铝片与稀盐酸反应 | B. | 氢氧化钡与氯化铵的反应 | ||
| C. | 灼热的碳与水蒸气的反应 | D. | 铝热反应 |
16.可逆反应2SO2+O2?2SO3 达到一定限度后通入18O2,再经过一段时间,18O存在于( )
| A. | SO2、O2中 | B. | SO3、SO2中 | C. | SO3中 | D. | SO3、SO2、O2中 |
17.原子序数依次增大的四种短周期元素a、b、c、d,a存在a+和a-两种离子,b和d为同一主族元素,b2-和c+的电子层结构相同,下列叙述正确的是( )
| A. | 元素的原子半径为d>c>b>a | |
| B. | b,d元素形成的最高价氧化物对应的水化物的酸性b>d | |
| C. | c与其它3种元素均能形成离子化合物 | |
| D. | a、b、c、d四种元素组成的化合物的水溶液可能为酸性、也可能为碱性 |
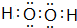 ,B的最高价氧化物的结构式:O=C=O.用电子式表示EF的形成过程
,B的最高价氧化物的结构式:O=C=O.用电子式表示EF的形成过程 .
.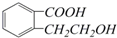 ,它可以通过不同的反应得到下列物质:
,它可以通过不同的反应得到下列物质: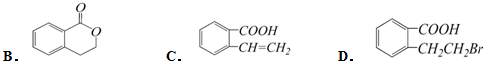
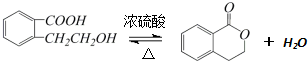 .
.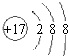
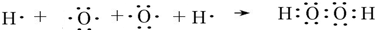
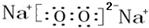 ,该化合物和B与D形成的某化合物反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2,1molH发生该反应转移电子数为6.02×1023
,该化合物和B与D形成的某化合物反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2,1molH发生该反应转移电子数为6.02×1023