题目内容
下列实验误差分析错误的是( )
| A、用容量瓶配制溶液时,定容时仰视刻度线,所配溶液浓度偏小 |
| B、用润湿的pH试纸测溶液的pH,所测pH不一定有误差 |
| C、测定中和反应的反应热时,将碱分多次倒入酸中,所测△H偏小 |
| D、酸碱中和滴定时,滴定前盛装标准液的滴定管内有气泡,终点读数时气泡消失,所测结果偏大 |
考点:中和滴定,测定溶液pH的方法,配制一定物质的量浓度的溶液
专题:
分析:A、用容量瓶配制溶液时,定容时仰视刻度线,读数偏小,溶液体积偏大;
B、用润湿的pH试纸测溶液的pH,相当于将原溶液稀释;
C、测定中和反应的反应热时,将碱分多次倒入酸中,造成热量散失过多;
D、酸碱中和滴定时,滴定前盛装标准液的滴定管内有气泡,终点读数时气泡消失,导致V(标准)偏大.
B、用润湿的pH试纸测溶液的pH,相当于将原溶液稀释;
C、测定中和反应的反应热时,将碱分多次倒入酸中,造成热量散失过多;
D、酸碱中和滴定时,滴定前盛装标准液的滴定管内有气泡,终点读数时气泡消失,导致V(标准)偏大.
解答:
解:A、溶液体积偏大时,配制溶液浓度减小,故A正确;
B、测定中性溶液的pH时,用润湿的pH试纸测溶液的pH无误差,故B正确;
C、热量散失过多,所测中和反应放热减少,放热越少△H越大,所以△H偏大,故C错误;
D、V(标准)偏大时,据c(待测)=
分析,测定结果偏大,故D正确;
故选C.
B、测定中性溶液的pH时,用润湿的pH试纸测溶液的pH无误差,故B正确;
C、热量散失过多,所测中和反应放热减少,放热越少△H越大,所以△H偏大,故C错误;
D、V(标准)偏大时,据c(待测)=
| c(标准)×V(标准) |
| V(待测) |
故选C.
点评:本题考查了配制一定物质的量浓度的溶液时的误差分析、pH试纸的使用、反应热测定实验、中和滴定实验误差分析,题目难度中等.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
NA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A、1mol甲基(-14C1H3)所含的中子数和电子数分别为8NA、9NA |
| B、标准状况下,11.2L氯仿中含有C-Cl键的数目为1.5NA |
| C、8.7gMnO2与40mL 10mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA |
| D、1 mol Na被完全氧化生成Na2O2,失去2 NA个电子 |
下列物质中属于电解质的是( )
| A、Cu |
| B、蔗糖 |
| C、Na2CO3 |
| D、乙醇 |
下列关于氧化还原反应的说法,正确的是( )
| A、氧化还原反应的特征是电子的转移 |
| B、氧化剂在反应中被还原,生成氧化产物 |
| C、同一反应中,氧化剂得电子的总数一定等于还原剂失电子的总数 |
| D、任何反应中一定有氧化剂和还原剂,且氧化剂和还原剂可以为同种物质 |
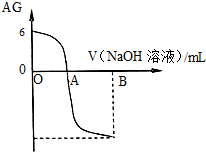 有人曾建议用AG表示溶液的酸度,AG的定义为:AG=lg
有人曾建议用AG表示溶液的酸度,AG的定义为:AG=lg| c(H+) |
| c(OH-) |
| A、A点时加入氢氧化钠溶液体积为20 mL |
| B、室温时0.01 mol/L的醋酸溶液pH=4 |
| C、OA段溶液中:c(CH3COO-)>c(CH3COOH) |
| D、若B点时加入NaOH溶液40 mL,所得溶液中:c(CH3COO-)+2 c(CH3COOH)+c(H+)=c(OH-) |