题目内容
A、B、C三种物质各15g,它们发生反应时,只生成30g新物质D.若增加10gC时,A与C恰好完全反应,则A与B参加反应质量之比为( )
| A、1:1 | B、2:1 |
| C、2:3 | D、3:2 |
考点:质量守恒定律
专题:
分析:若增加10gC时,A与C恰好完全反应,可计算出参加反应的A和C的质量比为;依此计算出原反应参加反应的A和B的质量关系.
解答:
解:若增加10gC时,A与C恰好完全反应,则参加反应的A的质量为15g,C的质量为25g,故参加反应的A和C的质量比为:15:25=3:5,
故A、B、C三种物质各15g,它们发生反应时,参加反应的C的质量为15g,A的质量为15g×
=9g,
根据质量守恒可知:参加反应的B的质量为30-15-9=6g,
故A与B参加反应的质量之比为:9:6=3:2,
故选D.
故A、B、C三种物质各15g,它们发生反应时,参加反应的C的质量为15g,A的质量为15g×
| 3 |
| 5 |
根据质量守恒可知:参加反应的B的质量为30-15-9=6g,
故A与B参加反应的质量之比为:9:6=3:2,
故选D.
点评:本题考查质量守恒定律定律,难度不大.要注意求算出参加反应的A和C的质量关系是解题的关键.

练习册系列答案
相关题目
下列反应属于吸热反应的是( )
| A、碳燃烧生成一氧化碳 |
| B、葡萄糖在人体内氧化分解 |
| C、锌粒与稀H2SO4反应制取H2 |
| D、Ba(OH)2?8H2O与NH4Cl(固体)反应 |
下列电离方程式的书写正确的是( )
| A、CuCl2=Cu+Cl2↑ |
| B、Na2CO3=2Na++CO32- |
| C、H2SO4=2H++S6++4O2- |
| D、NaHCO3=Na++H++CO32- |
将0.3mol/L盐酸100mL和0.6mol/L盐酸100mL放入500mL容量瓶中,然后加水稀释至刻度线,该溶液中H+的物质的量浓度为( )(mol/L)
| A、0.18 | B、0.3 |
| C、0.6 | D、0.45 |
下列化学式与指定物质的主要成分对应正确的是( )
| A、Fe2O3--磁性氧化铁 |
| B、CaO--生石灰 |
| C、NaHCO3--纯碱 |
| D、CuSO4--胆矾 |
短周期金属元素甲~戊在周期表中的相对位置如下表所示,下面判断不正确的是( )
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A、原子半径:丙<丁<戊 |
| B、金属性:甲<丙 |
| C、氢氧化物碱性:丙>丁>戊 |
| D、最外层电子数:甲>乙 |
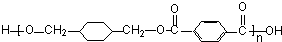
 -CH3+Cl2→
-CH3+Cl2→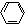 -CH2Cl+HCl
-CH2Cl+HCl