题目内容
3.下列说法中正确的是( )| A. | 活化分子具有的能量就是活化能 | |
| B. | 增大反应物浓度,可增大活化分子的百分数,从而使有效碰撞次数增大 | |
| C. | 无论是吸热反应还是放热反应,升高温度都能增大活化分子百分数 | |
| D. | 活化分子间的碰撞一定是有效碰撞 |
分析 A.活化能是活化分子高出反应物分子平均能量部分;
B.增大反应物浓度,活化分子的百分数不变;
C.升高温度分子吸收能量,分子总数不变的情况下,活化分子数目增多;
D.能发生化学反应的碰撞是有效碰撞.
解答 解:A.活化能是活化分子高出反应物分子平均能量部分,不是活化分子具有的总能量,故A错误;
B.增大反应物浓度,活化分子的数目增多,但是活化分子的百分数不变,故B错误;
C.升高温度分子吸收能量,分子总数不变的情况下,活化分子数目增多,所以升高温度都能增大活化分子百分数,故C正确;
D.能发生化学反应的碰撞是有效碰撞,活化分子在发生碰撞时取向合适才能发生反应,才属于有效碰撞,故D错误.
故选C.
点评 本题考查了有效碰撞理论,题目难度不大,注意把握活化能、活化分子、有效碰撞等概念,侧重于基础知识的考查.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
4.下列溶液中的氯离子浓度最大的是( )
| A. | 60mL 1mol•L-1氯化钠溶液 | B. | 75mL 1mol•L-1氯化钙溶液 | ||
| C. | 60mL 3mol•L-1氯化钾溶液 | D. | 75mL 1.5mol•L-1氯化铁溶液 |
14.在PH=1的透明溶液中能大量共存的离子组是( )
| A. | NH4+、K+、Cl-、HCO3- | B. | K+、Ba2+、OH-、NO3- | ||
| C. | Mg2+、Cu2+、Cl-、SO42- | D. | Na+、Cl-、Ba2+、SO32- |
11.如图所示,将铁棒和石墨棒插入1L 1mol•L-1食盐水中.下列说法正确的是( )
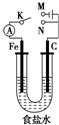

| A. | 若电键K与N连接,铁被保护不会腐蚀 | |
| B. | 若电键K与M连接,将石墨棒换成铜棒,可实现铁棒上镀铜 | |
| C. | 若电键K与N连接,正极反应式是 4OH--4e-═2H2O+O2↑ | |
| D. | 若电键K与M连接,当两极共产生22.4L(标准状况)气体时,生成了1mol NaOH |
18.亚硝酸(HNO2)既可作氧化剂又可作还原剂,当它在反应中作还原剂时,可能生成的产物是( )
| A. | N2 | B. | N2O3 | C. | NH3 | D. | NO2 |
8.R、X、Y和Z是四种元素,其在常见化合物中化合价均为+2价,且X2+与单质R不反应; X2++Z═X+Z2+;Y+Z2+=Y2++Z.这四种离子被还原成0价时表现的氧化性大小符合( )
| A. | X2+>R2+>Y2+>Z2+ | B. | Y2+>Z2+>R2+>X2+ | C. | Z2+>X2+>R2+>Y2+ | D. | R2+>X2+>Z2+>Y2+ |
15. 在一密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,如图表示该反应的速率(v)在某一时间段内的变化.则下列时间段中,SO3的百分含量最高的是( )
在一密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,如图表示该反应的速率(v)在某一时间段内的变化.则下列时间段中,SO3的百分含量最高的是( )
 在一密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,如图表示该反应的速率(v)在某一时间段内的变化.则下列时间段中,SO3的百分含量最高的是( )
在一密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,如图表示该反应的速率(v)在某一时间段内的变化.则下列时间段中,SO3的百分含量最高的是( )| A. | t0→t1 | B. | t2→t3 | C. | t3→t4 | D. | t3→t5 |
12.下列关于各图的说法,正确的是( )
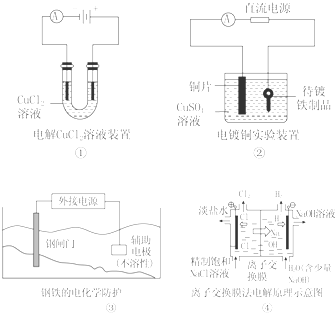

| A. | ①中阴极处能产生使湿润淀粉KI试纸变蓝的气体 | |
| B. | ②中待镀铁制品应与电源正极相连 | |
| C. | ③中钢闸门应与外接电源的正极相连 | |
| D. | ④中的离子交换膜可以避免生成的Cl2与NaOH溶液反应 |