题目内容
13.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 1molFeI2与1molCl2反应时转移的电子数为3NA | |
| B. | pH=1的H2SO4溶液,含H+的数目为NA | |
| C. | 273K、101kPa下,28g乙烯与丙烯混合物中含有氢原子总数数目为2NA | |
| D. | 2g H218O与D216O的混合物中所含中子、电子数目均为NA |
分析 A.1molFeI2与1molCl2反应时,1mol氯气完全反应最多得到2mol电子;
B.没有告诉硫酸溶液的体积,无法计算溶液中含有氢离子的数目;
C.乙烯和丙烯的最简式为CH2,根据最简式计算出混合物中含有H原子数目;
D.H218O与D216O摩尔质量都是20g/mol,二者分子中都含有10个中子,据此计算出2g H218O与D216O含有的中子、电子数.
解答 解:A.1molFeI2与1molCl2反应时,1mol氯气完全反应最多得到2mol电子,转移的电子数为2NA,故A错误;
B.没有告诉pH=1的硫酸溶液的体积,无法计算溶液中含有氢离子的物质的量,故B错误;
C.28g乙烯与丙烯混合物中含有28最简式CH2,含有最简式CH2的物质的量为:$\frac{28g}{14g/mol}$=2mol,则该混合物中含有4molH原子,含有氢原子总数数目为4NA,故C错误;
D.2g H218O与D216O的物质的量都是:$\frac{2g}{20g/mol}$=0.1mol,H218O与D216O中含有的电子、中子数都是10,则二者含有的中子、电子的物质的量都是1mol,所以混合物中所含中子、电子数目均为NA,故D正确;
故选D.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,B为易错点,注意题中缺少溶液体积,试题培养了学生的化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.苄基(C6H5CH2-)、-OH、-CHO、-COOH四种基团,它们之间两两组合,所形成的有机物有( )
| A. | 3 种 | B. | 4种 | C. | 5种 | D. | 6种 |
1.下列有关溶液的说法正确的是( )
| A. | 将质量分数为40%(密度为1.43g•cm-3)的NaOH溶液与等体积水混合,所得溶液中溶质的质量分数是20% | |
| B. | 要配制浓度为0.25mol•L-1的NaOH溶液480mL,应称量4.8gNaOH在250mL的烧杯中溶解,冷却,再转移到500mL容量瓶中,洗涤、转移、定容 | |
| C. | 配制一定物质的量浓度的溶液,定容时俯视刻度线导致所配浓度偏高 | |
| D. | 配制NaOH溶液,在烧杯中溶解NaOH后未冷却至室温就转移到容量瓶中,溶液浓度偏低 |
8.科学研究发现,具有高度对称性的有机分子具有致密性高,稳定性强,张力能大等特点,因此这些分子成为2014年化学界关注的热点,下面是几种常见高度对称烷烃的分子碳架结构这三种烷烃的二氯取代产物的同分异构体数目是( )
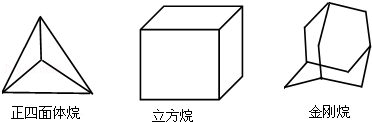

| A. | 2种 4种 8种 | B. | 2种 4种 6种 | C. | 1种 3种 6种 | D. | 1种 3种 8种 |
5.下列各物质中,能发生加成反应的是( )
| A. | 天然气 | B. | 苯 | C. | 沼气 | D. | 瓦斯 |
3.实验室有两瓶失去标签的溶液,其中一瓶是KHSO4溶液,另一瓶是KOH溶液.鉴别时,下列选用的试纸或试剂不正确的是( )
| A. | pH试纸 | B. | 紫色石蕊试液 | C. | K2CO3固体 | D. | KCl溶液 |