题目内容
8.某学习小组根据SO2的性质进行如下相关实验研究.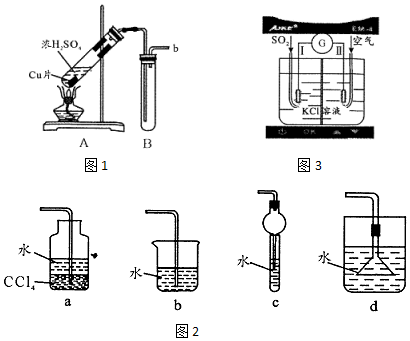
【制备SO2】按照如图1装置制备SO2.
(1)A试管中可观察到的现象是铜片逐渐溶解,有无色气体逸出,试管底部出现灰白色固体;SO2具有漂白性,试再举出两种漂白原理互不相同的物质活性炭;臭氧、次氯酸.
(2)若A试管中只加浓硫酸,加热过程中,导管b出口处的气体遇见潮湿的空气会有少量“酸雾”产生.推测b处出现酸雾的主要化学反应方程式为SO3+H2O=H2SO4.
(3)SO2尾气可以用浓氨水吸收.实验室制备NH3的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;图2装置中宜用于NH3制备浓氨水的是ac(填序号).
【SO2浓度检测】
(4)学生用ME3-SO2型电化学传感器测量试管B中SO2气体浓度,工作原理如图3.电极Ⅱ的反应式为O2+4H++4e-═2H2O;当通入VmL气体时,测得SO2浓度为amol/L.此时电解液中生成的n(H+)为2Va×10-3mol;
电化学传感器灵敏度受温度影响.若高于工作温度时,测得SO2,浓度可能偏低,其原因可能是温度升高,吸附在电极上的SO2减少,导致测得结果偏低.
分析 【制备SO2】(1)浓硫酸具有强氧化性和吸水性,铜和热的浓硫酸发生氧化还原反应生成硫酸铜、二氧化硫和水,硫酸铜固体为白色粉末,据此分析解答;臭氧、漂白粉、次氯酸漂白原理相同,都是因为具有强氧化性,能氧化有机色素而具有漂白性,二氧化硫能够与有机色素化合生成无色物质而具有漂白性,活性炭具有较大的表面积,具有吸附作用而具有漂白极性;
(2)硫酸受热分解生成三氧化硫和水,三氧化硫和水蒸气结合生成酸雾;
(3)实验室制备NH3,用氯化铵固体和氢氧化钙固体在加热的条件下发生反应生成氨气;氨气极易溶于水,若吸收时导管伸入水中,由于气体溶于水,导致装置内压强急剧降低,外界大气压压着液体进入,产生倒吸现象,据此分析NH3制备浓氨水的装置;
【SO2浓度检测】
(4)原电池负极发生氧化反应,SO2被氧化生成SO42-,在氯化钾溶液中,正极氧气得到电子发生还原反应生成氢氧根离子,根据总方程式可知n(H+)=2n(H2SO4)=2n(SO2)=,据此计算生成的n(H+),气体的溶解度受温度的影响,温度高溶解度小.
解答 解:(1)A试管中铜和热的浓硫酸发生氧化还原反应生成硫酸铜、二氧化硫和水,反应为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,所以现象为:铜片逐渐溶解,有无色气体逸出(SO2),试管底部出现灰白色固体(硫酸铜固体),二氧化硫具有漂白作用,利用二氧化硫和水反应生成的亚硫酸和有机色素结合为不稳定的无色物质,二氧化硫为化合漂白,活性炭具有较大的表面积,为吸附性漂白,臭氧、次氯酸具有漂白作用,利用的是强氧化性,它们漂白原理互不相同,
故答案为:铜片逐渐溶解,有无色气体逸出,试管底部出现灰白色固体;活性炭;臭氧、次氯酸;
(2)若A试管中只加浓硫酸,加热过程中,硫酸受热分解生成三氧化硫和水,导管b出口处的气体遇见潮湿的空气会有少量“酸雾”产生,是三氧化硫和水蒸气结合生成的酸雾,反应为:SO3+H2O=H2SO4,
故答案为:SO3+H2O=H2SO4;
(3)铵盐和碱反应生成氨气,实验室用氯化铵固体和氢氧化钙固体在加热的条件下制备NH3,反应的方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,
a、氨气难溶于四氯化碳,逸出四氯化碳层进入水层,被水吸收,不易产生倒吸,故a正确;
b、氨气极易溶于水,导管直接伸入到液体中,由于气体溶于水,导致装置内压强急剧降低,外界大气压压着液体进入,不能防止倒吸,故b错误;
c、氨气极易溶于水,吸收装置中的导管外联双球状导管内伸入到液体中,能防止倒吸,故c正确;
d、氨气极易溶于水,吸收装置中的倒扣漏斗没入到液体中,不能防止倒吸,故d错误.
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;ac;
(4)原电池负极发生氧化反应,SO2被氧化生成SO42-,电极I电极反应式为SO2+2H2O-2e-=SO42-+4H+,通入氧气的一极为正极,得电子发生还原反应,电极Ⅱ电极方程式为O2+4H++4e-═2H2O,电池的总反应式为:2SO2+2H2O+O2=2H2SO4,n(H+)=2n(H2SO4)=2n(SO2)=2Va×10-3mol,若高于工作温度时,测得SO2,浓度可能偏低,是因为温度升高,吸附在电极上的SO2减少,导致测得结果偏低,
故答案为:O2+4H++4e-═2H2O;2Va×10-3mol;温度升高,吸附在电极上的SO2减少,导致测得结果偏低.
点评 本题考查SO2的性质实验,掌握硫、氮及其化合物的性质以及原电池工作原理是解答关键,注意不同的防止倒吸装置的原理,题目难度中等,试题充分考查了学生的分析、理解能力及化学实验能力.

| A. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | B. | Cu(OH)2+2HCl═CuCl2+2H2O | ||
| C. | CuO+2HCl═CuCl2+H2O | D. | NH4Cl+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+NH3↑+H2O |
| A. | 含NA个阴离子的Na2O2溶于水形成1L溶液,其物质的量浓度为2mol/L | |
| B. | 25g质量分数为68%的H2O2水溶液中含有氧原子数目为NA | |
| C. | 标准状况下,22.4L H2O含有的分子数为NA | |
| D. | 用5mL 3mol/L FeCl3溶液制成的氢氧化铁胶体中所含胶粒数为0.015NA |
| A. | 取代反应 | B. | 加成反应 | C. | 氧化反应 | D. | 还原反应 |
 将Na2O2加入含有Al3+、Fe2+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示.下列说法不正确的是( )
将Na2O2加入含有Al3+、Fe2+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示.下列说法不正确的是( )| A. | a=1.75 | |
| B. | b=0.5 | |
| C. | 原溶液中Al3+与Fe2+的物质的量之比为1:2 | |
| D. | 最后得到的沉淀为Fe(OH)3 |
| A. | Cl2 | B. | KNO3 | C. | SO2 | D. | Al |
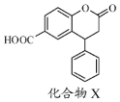
| A. | 分子中两个苯环一定处于同一平面 | |
| B. | 不能与饱和Na2CO3溶液反应 | |
| C. | 1 mol化合物X最多能与2 molNaOH反应 | |
| D. | 在酸性条件下水解,水解产物只有一种 |