题目内容
4.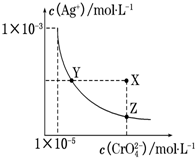 在t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示. 又知AgCl的Ksp=1.8×10-10.下列说法正确的是( )
在t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示. 又知AgCl的Ksp=1.8×10-10.下列说法正确的是( )| A. | t℃时,Ag2CrO4的Ksp为1×10-8 | |
| B. | 在饱和Ag2CrO4溶液中加入K2CrO4能使溶液由Y点变为X点 | |
| C. | t℃时,Y点和Z点时Ag2CrO4的Ksp相等 | |
| D. | t℃时,将0.01 mol•L-1 AgNO3溶液滴入20 mL 0.01 mol•L-1 KCl和0.01 mol•L-1 K2CrO4的混合溶液中,CrO42-先沉淀 |
分析 A.t℃时,Ag2CrO4的Ksp=c2(Ag+)c(CrO42-);
B.饱和Ag2CrO4溶液中加入K2CrO4,c(CrO42-)增大,平衡逆向移动,c(Ag+)减小;
C.Ksp只与温度有关;
D.结合Ksp及c(Ag+)计算阴离子浓度,阴离子浓度小的先沉淀.
解答 解:A.t℃时,Ag2CrO4的Ksp=c2(Ag+)c(CrO42-)=(1×10-3)2×(1×10-5)=1×10-11,故A错误;
B.饱和Ag2CrO4溶液中加入K2CrO4,c(CrO42-)增大,平衡逆向移动,c(Ag+)减小,则Y点变为X点时c(Ag+)不变、c(CrO42-)增大,故B错误;
C.Ksp只与温度有关,则t℃时,Y点和Z点时Ag2CrO4的Ksp相等,故C正确;
D.c(Cl-)=$\frac{1.8×1{0}^{-10}}{0.01}$=1.8×10-8,c(CrO42-)=$\frac{1×1{0}^{-11}}{(0.01)^{2}}$=1×10-7,Cl-先沉淀,故D错误;
故选C.
点评 本题考查难溶电解质的溶解平衡,为高频考点,把握溶解平衡移动、Ksp的计算为解答的关键,侧重分析与应用能力的考查,注意Ksp只与温度有关,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.下列说法正确的是( )
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 化学反应中的能量变化都表现为热量变化 | |
| C. | 可逆反应达到化学平衡时,正、逆反应速率都为0 | |
| D. | 反应物和生成物所具有的总能量决定了反应是放热还是吸热 |
18.下列离子方程式书写正确的是( )
| A. | 氢氧化钠溶液和稀盐酸反应:H++OH-═H2O | |
| B. | 大理石与盐酸反应制取二氧化碳:CO32-+2H+═H2O+CO2↑ | |
| C. | 铁粉投入盐酸溶液中:2Fe+6H+═Fe3++3H2↑ | |
| D. | 用小苏打治疗胃酸过多:CO32-+2H+═CO2↑+H2O |
12.表是0.1mol/L的部分阳离子常温下以氢氧化物形式沉淀时溶液的pH:
判断下列说法中正确的是( )
| 阳离子 | Fe3+ | Fe2+ | Cu2+ |
| 开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
| A. | 在含有Fe2+、Fe3+、Cu2+的混合溶液中,滴加氢氧化钠溶液时Fe2+先产生沉淀 | |
| B. | 在含有Fe2+、Fe3+、Cu2+的混合溶液中,若除去混合溶液中的Fe2+、Fe3+,可先加入稀硝酸,再加入氧化铜调节溶液的pH的范围为3.2-4.7 | |
| C. | 相同温度下,Ksp[(Cu(OH)2)>Ksp[(Fe(OH)2) | |
| D. | 在含有Fe2+、Fe3+、Cu2+的混合溶液中,除去混合溶液中的Fe2+、Fe3+,可加入足量的铁粉 |
9.对于已达到平衡的可逆反应:A(g)?2B(?)+C(g)△H>0,假设A、C状态保持不变,下列说法正确的是( )
| A. | 当混合气体的质量不变,说明反应已达平衡状态 | |
| B. | 缩小容器体积,重新达到平衡时,气体混合物中C%可能增大 | |
| C. | 在恒压容器中升高温度,气体混合物中C%可能先增大后减小 | |
| D. | 在恒容容器中升高温度,达到新平衡时,气体的密度增大 |
16.在溶液中有浓度均为0.01mol•L-1的Fe3+、Cr3+、Zn2+、Mg2+等离子,已知:25℃时,Ksp[Fe(OH)3]=4.0×10-38;Ksp[Cr(OH)3]=7.0×10-31,Ksp[Zn(OH)2]=1.0×10-17;Ksp[Mg(OH)2]=1.8×10-11.当其氢氧化物刚开始沉淀时,下列哪一种离子所需的pH最小( )
| A. | Fe3+ | B. | Cr3+ | C. | Zn2+ | D. | Mg2+ |
14.下列氯化物不能用金属与盐酸反应得到的是( )
①FeCl3 ②FeCl2③CuCl2 ④MgCl2.
①FeCl3 ②FeCl2③CuCl2 ④MgCl2.
| A. | ①②③ | B. | ①③ | C. | ②④ | D. | ①④ |