题目内容
17.写出下列盐溶液水解的离子方程式:(1)NH4ClNH4++H2O?NH3•H2O+H+;
(2)NaClOClO-+H2O?HClO+OH-;
(3)KAl(SO4)2Al3++3H2O?Al(OH)3+3H+;
(4)Na2SO3SO32-+H2O?HSO3-+OH-.
分析 (1)氯化铵水解呈酸性,生成一水合氨;
(2)NaClO为强碱弱酸盐,水解呈碱性,生成HClO;
(3)KAl(SO4)2 含有铝离子,可水解呈酸性;
(4)Na2SO3为强碱弱酸盐,水解呈碱性.
解答 解:(1)氯化铵水解呈酸性,生成一水合氨,水解的离子方程式为NH4++H2O?NH3•H2O+H+,故答案为:NH4++H2O?NH3•H2O+H+;
(2)NaClO为强碱弱酸盐,水解呈碱性,生成HClO,水解的离子方程式为ClO-+H2O?HClO+OH-,故答案为:ClO-+H2O?HClO+OH-;
(3)KAl(SO4)2 含有铝离子,可水解呈酸性,水解的离子方程式为Al3++3H2O?Al(OH)3+3H+,故答案为:Al3++3H2O?Al(OH)3+3H+;
(4)Na2SO3为强碱弱酸盐,水解呈碱性,水解的离子方程式为SO32-+H2O?HSO3-+OH-,故答案为:SO32-+H2O?HSO3-+OH-.
点评 本题考查了盐类的水解的离子方程式的书写,题目难度中等,注意掌握盐的水解原理,然后根据“谁弱谁水解”、“谁强谁显性”来分析解答即可.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
7.已知:I2+2S2O32-═S4O62-+2I-.
相关物质的溶度积常数见表:
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2•2H2O,加入CuO,调至pH=4,使溶液
中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=2.6×10-9mol/L.过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2•2H2O.
(2)在空气中直接加热CuCl2•2H2O得不到纯的无水CuCl2,原因是2CuCl2•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Cu(OH)2•CuCl2+2HCl+2H2O(用化学方程式表示).
(3)某学习小组用“间接碘量法”测定含有CuCl2•2H2O的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀(发生反应:2Cu2++4I-═2CuI↓+I2).用0.100 0mol•L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.
①可选用淀粉溶液作滴定指示剂,滴定终点的现象是溶液蓝色褪去,且半分钟内不变色.
②该试样中CuCl2•2H2O的质量分数为95%.
相关物质的溶度积常数见表:
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=2.6×10-9mol/L.过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2•2H2O.
(2)在空气中直接加热CuCl2•2H2O得不到纯的无水CuCl2,原因是2CuCl2•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Cu(OH)2•CuCl2+2HCl+2H2O(用化学方程式表示).
(3)某学习小组用“间接碘量法”测定含有CuCl2•2H2O的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀(发生反应:2Cu2++4I-═2CuI↓+I2).用0.100 0mol•L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.
①可选用淀粉溶液作滴定指示剂,滴定终点的现象是溶液蓝色褪去,且半分钟内不变色.
②该试样中CuCl2•2H2O的质量分数为95%.
8.关于乙醇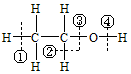 在化学反应中断键位置说法错误的是( )
在化学反应中断键位置说法错误的是( )
 在化学反应中断键位置说法错误的是( )
在化学反应中断键位置说法错误的是( )| A. | 乙醇与钠反应,在④位置断裂,对比钠与水反应,乙醇比水更难电离出氢离子 | |
| B. | 乙醇与浓硫酸在170℃时,在②③位置断裂,以水分子的形式消去,属于消去反应 | |
| C. | 乙醇与浓硫酸在140℃时,在③或④位置断裂,该反应是取代反应 | |
| D. | 乙醇在铜催化下与氧气反应,在②④位置断裂,所以只有与羟基直接相连的碳原子上有氢原子才能发生催化氧化 |
5.下列说法中正确的是( )
| A. | 由同种分子构成的物质一定是纯净物 | |
| B. | 纯净物一定由分子构成 | |
| C. | 混合物肯定是由两种以上的元素组成的 | |
| D. | 含有氧元素的化合物就是氧化物 |
2.已知:相同温度下Ka(HF)>Ka(HCN).现有物质的量浓度和体积均相同的NaF和NaCN两种溶液,已知前者溶液中所含离子数目为n1,后者溶液中所含离子数目为n2,下列关系正确的是( )
| A. | 溶液pH:NaF>NaCN | B. | n1>n2 | ||
| C. | H2O的电离程度:NaF>NaCN | D. | c(F-)<c(CN-) |
9.下列叙述不正确的是( )
| A. | 异戊二烯分子里的所有原子不可能在同一平面上 | |
| B. | 浓氨水洗涤做过银镜反应的试管 | |
| C. | 油脂皂化反应得到高级脂肪酸盐与甘油 | |
| D. | 聚合物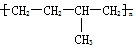 可由单体CH3CH=CH2和CH2=CH2加聚制得 可由单体CH3CH=CH2和CH2=CH2加聚制得 |
6.下列叙述正确的是( )
| A. | 1 mol H2SO4的质量是98 g/mol | |
| B. | CO2的摩尔质量等于CO2的相对分子质量 | |
| C. | 摩尔质量建立了物质的物质的量与物质的质量之间的联系 | |
| D. | 1 mol任何物质的质量等于该物质的相对分子质量 |
8.某课外兴趣小组用0.10mol•L-1标准盐酸滴定某NaOH溶液的浓度,用酚酞作指示剂.
①滴定终点时的现象为锥形瓶中的溶液由红色变无色且在半分钟内不恢复;
②滴定时边滴边摇动锥形瓶,眼睛应观察锥形瓶内溶液颜色的变化;
③下列操作可能使测定结果偏低的是C.
A.酸式滴定管在装酸液前未用标准酸液润洗
B.开始时酸式滴定管尖嘴部分留有气泡,滴定过程中消失
C.装待测液的滴定管,放液前平视,后仰视
D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次
④已知测的下列数据:
则待测烧碱溶液的物质的量浓度为0.08mol/L.
①滴定终点时的现象为锥形瓶中的溶液由红色变无色且在半分钟内不恢复;
②滴定时边滴边摇动锥形瓶,眼睛应观察锥形瓶内溶液颜色的变化;
③下列操作可能使测定结果偏低的是C.
A.酸式滴定管在装酸液前未用标准酸液润洗
B.开始时酸式滴定管尖嘴部分留有气泡,滴定过程中消失
C.装待测液的滴定管,放液前平视,后仰视
D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次
④已知测的下列数据:
| 测定次数 | 待测液体积/mL | 标准盐酸体积/mL | |
| 滴定前读数/mL | 滴定后读数/mL | ||
| 第一次 | 25.00 | 0.40 | 20.38 |
| 第二次 | 25.00 | 4.00 | 24.02 |