题目内容
(14分)(1)用稀硫酸浸泡由黄铜矿(主要成分CuFeS2)冶炼铜得到的滤渣,取少量所得溶液,滴加KSCN溶液后呈红色,则溶液中存在 (离子符号)。
写出上述反应的离子方程式:_______ _________。
(2)铜在自然界存在于多种矿石中,如
矿石名称 | 黄铜矿 | 斑铜矿 | 辉铜矿 | 孔雀石 |
主要成分 | CuFeS2 | Cu5 FeS4 | Cu2S | CuCO3·Cu(OH)2 |
请回答下列问题:
①上表所列铜化合物中,铜的质量百分含量最高的是 (填化学式)。
②工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。该工艺的中间过程会发生反应:2Cu2O+Cu2S 6Cu+SO2↑(Cu2S中S的化合价为-2),该反应的氧化剂是__________。若此反应得到64克铜,则过程中转移的电子数________。
6Cu+SO2↑(Cu2S中S的化合价为-2),该反应的氧化剂是__________。若此反应得到64克铜,则过程中转移的电子数________。
(1)Fe3+ Fe3++ 3SCN-≒Fe(SCN)3 (2) ①Cu2S ② Cu2O、Cu2S NA或6.02×1023
【解析】
试题分析:(1)能使KSCN溶液变红的是Fe3+,它们发生反应的离子方程式为:Fe3++ 3SCN-≒Fe(SCN)3(2)①不用每个物质都去计算铜的质量分数,可以把Cu的个数都变成1个,再比较剩余部分的相对原子质量的大小,剩余部分相对原子质量越小,铜的质量分数越高,可变为:CuFeS2、Cu( FeS4)1/5、CuS1/2 、Cu (CO3 )1/2(OH),可以看出S1/2的相对原子质量最小,所以Cu2S中的铜的质量分数最高。②从反应的化合价来看,铜从1+价变为0价,化合价降低,那么含Cu的物质做氧化剂,所以氧化剂有Cu2O和Cu2S,反应中转移的电子数为6e-,64克铜的物质的量为:64g÷64g/mol=1mol,设转移电子物质的量为n,则有:
2Cu2O + Cu2S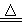 6Cu + SO2↑ 6e-
6Cu + SO2↑ 6e-
6 6
1mol n 得n=1mol,那么电子数为:NA或6.02×1023
考点:离子方程式的书写和氧化还原反应中的基本概念,电子转移的计算。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案(8分)研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)一定条件下,将2molNO与2molO2置于恒容密闭容器中发生反应2NO(g)+O2(g) 2NO2(g),下列各项能说明反应达到平衡状态的是 。
2NO2(g),下列各项能说明反应达到平衡状态的是 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.NO和O2的物质的量之比保持不变
d.每消耗1 molO2同时生成2 molNO2
(2)CO可用于合成甲醇,一定温度下,向体积为2L的密闭容器中加入CO和H2,发生反应CO(g)+2H2(g) CH3OH(g),达平衡后测得各组分浓度如下:
CH3OH(g),达平衡后测得各组分浓度如下:
物质 | CO | H2 | CH3OH |
浓度(mol?L—1) | 0.9 | 1.0 | 0.6 |
①列式并计算平衡常数K=__________________________。
②若降低温度,K值增大,则反应的△H 0(填“>”或“<”)。
③若保持体积不变,再充入0.6molCO和0.4molCH3OH,此时v正___v逆(填“>”、“<”或“=”)