题目内容
已知十水碳酸钠溶于水时溶液温度升高,室温下将1mol碳酸钠制成溶液时放出热量为Q1 kJ,又知十水碳酸钠分解的热化学方程式为:Na2CO3·10H2O(s)  Na2CO3 (s)+10H2O(1) △H = +Q2kJ/mol(Q2>0)则Q1和Q2的关系为( )
Na2CO3 (s)+10H2O(1) △H = +Q2kJ/mol(Q2>0)则Q1和Q2的关系为( )
A.Q1>Q2 B.Q1<Q2 C.Q1=Q2 D.无法确定
练习册系列答案
相关题目
高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) △H=aKJ ·mol-1
2Fe(s)+3CO2(g) △H=aKJ ·mol-1
(1)已知:
①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H1=+489.0kJ·mol-1
C(石墨)+CO2(g)=2CO(g) △H2=+172.5kJ·mol-1
则a= kJ·mol-1。
(2)冶炼铁反应的平衡常数表达式K= ,温度升高后,K值 (填“增大”、“不变”或“减小”)。
(3)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
Fe2O3 | CO | Fe | CO2 | ||
甲/mol | 1.0 | 1.0 | 1.0 | 1.0 | |
乙/mol | 1.0 | 2.0 | 1.0 | 1.0 | |
甲容器中CO的平衡转化率为 。
②下列说法正确的是 (填字母)。
a.若容器内气体密度恒定时,标志反应达到平衡状态
b.甲、乙容器中,CO的平衡浓度之比为2:3
c.增加Fe2O3可以提高CO2的转化率


 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则: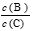 将_________。
将_________。 C(g)+D(g) △H >0。在相同温度下反应达到平衡,活塞移动到4处。下列有关说法正确的是( )
C(g)+D(g) △H >0。在相同温度下反应达到平衡,活塞移动到4处。下列有关说法正确的是( )