��Ŀ����
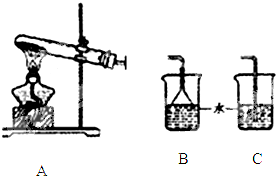 ij�о���ѧϰС��Ϊ����ȡ��̽�����������ʣ���������ʵ�飮[װ��A�з�����Ӧ�Ļ�ѧ����ʽ��2NH4Cl+Ca��OH��2
ij�о���ѧϰС��Ϊ����ȡ��̽�����������ʣ���������ʵ�飮[װ��A�з�����Ӧ�Ļ�ѧ����ʽ��2NH4Cl+Ca��OH��2
| ||
[��ȡ����]
��1��װ��A�еķ�Ӧ
��2��ʵ������װ��A��������ȡ��������
��3���ռ��������������ſ�����������Ϊ�������ܶȱȿ������ܶ�
��4����5.35gNH4Cl���壬�����Ƶ�NH3�����ʵ�����
[ʵ��̽��]
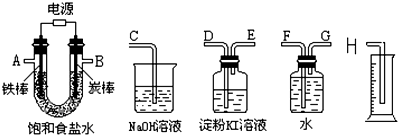
��5����֪������������ˮ��Ϊ�����հ���Ӧѡ���װ����
��6����ˮ�еμӼ��η�̪��Һ����ˮ��
��7������֧�ֱ�պȡŨ��ˮ��Ũ����IJ��������������Թ۲쵽������֮����ִ���
[֪ʶ��չ]
��8����ʯ����ˮ��Ӧ����Ca��OH��2���ų�����[��ѧ����ʽΪCaO+H2O�TCa��OH��2]��ʵ�������ô�ԭ��������ʯ��ˮ�μ�Ũ��ˮ�����Կ�����ȡ��������ʯ�ҿ�������
�ټ�ʯ�ң�NaOH��CaO�Ĺ������ ��ʯ��ʯ��CaCO3��
[֪ʶӦ��]
��9��������һ����Ҫ�Ļ���ԭ�ϣ�����д������һ����;��
���㣺������ȡ������
ר�⣺����Ԫ��
��������1��װ��A�����Ȼ�狀��������ƻ�ϼ��ȷ�Ӧ���ɰ����ĸ��ֽⷴӦ����������ԭ��Ӧ��
��2��ʵ�����Ʊ��������ù���+������ȷ�Ӧ���ɣ�
��3�������ܶ�С�ڿ�����
��4�����ݵ�Ԫ���غ�������ɰ����������
��5�����ռ�������ˮ����������õ�����Һ���©����ֹ������
��6����ˮ��Һ��һˮ�ϰ������������������ӣ���Һ�ʼ��ԣ�
��7���������Ȼ��ⷴӦ���ɹ����Ȼ�泥�
��8����ʯ���������ƺ��������ƹ������
��9�����ݰ���ѡ�����;��������ҵ���Ʊ����ᣬ��������ȣ�
��2��ʵ�����Ʊ��������ù���+������ȷ�Ӧ���ɣ�
��3�������ܶ�С�ڿ�����
��4�����ݵ�Ԫ���غ�������ɰ����������
��5�����ռ�������ˮ����������õ�����Һ���©����ֹ������
��6����ˮ��Һ��һˮ�ϰ������������������ӣ���Һ�ʼ��ԣ�
��7���������Ȼ��ⷴӦ���ɹ����Ȼ�泥�
��8����ʯ���������ƺ��������ƹ������
��9�����ݰ���ѡ�����;��������ҵ���Ʊ����ᣬ��������ȣ�
���
�⣺��1��װ��A�����Ȼ�狀��������ƻ�ϼ��ȷ�Ӧ���ɰ�������Ӧǰ����Ԫ�ػ��ϼ۱仯���ڷ�������ԭ��Ӧ���Ǹ��ֽⷴӦ������������ԭ��Ӧ��
�ʴ�Ϊ�����ǣ�
��2��ʵ�����Ʊ��������ù���+������ȷ�Ӧ���ɣ�����װ��ͼ��Ҫ���Ʊ��������ĺ�ϡ���ᷴӦ����Ӧ������ȣ�
�ʴ�Ϊ��O2��
��3���ռ��������������ſ�����������Ϊ�������ܶȱȿ������ܶ�С��
�ʴ�Ϊ��С��
��4�����ݵ�Ԫ���غ�������ɰ������������5.35gNH4Cl�������ʵ���=
=0.1mol�������Ƶ�NH3�����ʵ���Ϊ0.1mol��
�ʴ�Ϊ��0.1��
��5�����ռ�������ˮ����������õ�����Һ���©����ֹ������
�ʴ�Ϊ��B��
��6����ˮ��Һ��һˮ�ϰ������������������ӣ���Һ�ʼ��ԣ���ˮ�еμӼ��η�̪��Һ����ˮ���ɫ��
�ʴ�Ϊ���죻
��7���������Ȼ��ⷴӦ���ɹ����Ȼ�泥�����֧�ֱ�պȡŨ��ˮ��Ũ����IJ�����������Ũ��ˮ�ӷ����İ�����Ũ����ӷ������Ȼ���������Ӧ�����Թ۲쵽������֮����ִ������̣�
�ʴ�Ϊ�����̣�
��8����ʯ���������ƺ��������ƹ�������μ�Ũ��ˮ�����Կ�����ȡ������
�ʴ�Ϊ���٣�
��9�����ݰ���ѡ�����;��������ҵ���Ʊ����ᣬ����������Ʊ����ʵȣ�
�ʴ�Ϊ����ҵ���Ʊ����ᣬ����������Ʊ����ʵȣ�
�ʴ�Ϊ�����ǣ�
��2��ʵ�����Ʊ��������ù���+������ȷ�Ӧ���ɣ�����װ��ͼ��Ҫ���Ʊ��������ĺ�ϡ���ᷴӦ����Ӧ������ȣ�
�ʴ�Ϊ��O2��
��3���ռ��������������ſ�����������Ϊ�������ܶȱȿ������ܶ�С��
�ʴ�Ϊ��С��
��4�����ݵ�Ԫ���غ�������ɰ������������5.35gNH4Cl�������ʵ���=
| 5.35g |
| 53.5g/mol |
�ʴ�Ϊ��0.1��
��5�����ռ�������ˮ����������õ�����Һ���©����ֹ������
�ʴ�Ϊ��B��
��6����ˮ��Һ��һˮ�ϰ������������������ӣ���Һ�ʼ��ԣ���ˮ�еμӼ��η�̪��Һ����ˮ���ɫ��
�ʴ�Ϊ���죻
��7���������Ȼ��ⷴӦ���ɹ����Ȼ�泥�����֧�ֱ�պȡŨ��ˮ��Ũ����IJ�����������Ũ��ˮ�ӷ����İ�����Ũ����ӷ������Ȼ���������Ӧ�����Թ۲쵽������֮����ִ������̣�
�ʴ�Ϊ�����̣�
��8����ʯ���������ƺ��������ƹ�������μ�Ũ��ˮ�����Կ�����ȡ������
�ʴ�Ϊ���٣�
��9�����ݰ���ѡ�����;��������ҵ���Ʊ����ᣬ����������Ʊ����ʵȣ�
�ʴ�Ϊ����ҵ���Ʊ����ᣬ����������Ʊ����ʵȣ�
���������⿼���˰��������ʷ���Ӧ�ã�ʵ�����Ʊ�������ע��ʵ���������������Ӧ�úͰ������ʵ����������ǽ���ؼ�����Ŀ�ϼ�

��ϰ��ϵ�д�
�����Ŀ
��������˳����ȷ���ǣ�������
�����ԣ�H3PO4��H2SO4��HClO4��
�����ȶ��ԣ�H2O��HF��H2S����
��ԭ�Ӱ뾶��Na��Mg��O
�ܻ�ԭ�ԣ�F-��Cl-��S2-��
�ݽ��H+��������OH-��CH3COO-��Cl-��
�����ԣ�H3PO4��H2SO4��HClO4��
�����ȶ��ԣ�H2O��HF��H2S����
��ԭ�Ӱ뾶��Na��Mg��O
�ܻ�ԭ�ԣ�F-��Cl-��S2-��
�ݽ��H+��������OH-��CH3COO-��Cl-��
| A���ۢ� | B���ڢ� |
| C���٢ۢ� | D���ڢܢ� |
����˵����ȷ���ǣ�������
| A����100�桢101 KPa�����£�1molҺ̬ˮ����Ϊˮ�������յ�����Ϊ40.69KJ����H2O��g��?H2O��l�� �ġ�H=-40.69KJ/mol |
| B����֪MgCO3��Ksp=6.82��10-4mol2/L2�������к�����MgCO3����Һ�У�����C��Mg 2+ ��=C��CO32-������ C��Mg2+��?C��CO32-��=6.82��10-4mol2/L2 |
| C����֪��C-C�ļ���348KJ/mol��C=C�ļ���610KJ/mol��C-H�ļ���413KJ/mol�� H-H�ļ���436KJ/mol�� 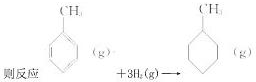 ���ʱ�Ϊ����H=[��4��348+3��610+8��413��+3��436-��7��348+14��413��]=-384 kJ/mol ���ʱ�Ϊ����H=[��4��348+3��610+8��413��+3��436-��7��348+14��413��]=-384 kJ/mol |
| D��̼��������Һ�д��ڣ�c��H*��+c��H2CO3��=c��OH-��+c��CO32-�� |
����1.0mol/L��NaOH��Һ0.1L����ͨ���״�������Ϊ2.24L ��SO2���壬ʹ���ַ�Ӧ����������Һ�и�����Ũ�ȴ�С��ϵ��ȷ���ǣ�������
| A��c��Na+��+c��H+��=c��HSO3-��+c��SO32-��+c�� OH-�� |
| B��c��Na+��=c��H2SO3��+c��HSO3-��+c�� H+�� |
| C��c��SO32-��+c�� OH-��=c��H+��+c��H2SO3�� |
| D��c��Na+����c��HSO3-����c�� OH-����c��H2SO3����c��SO32-����c��H+�� |
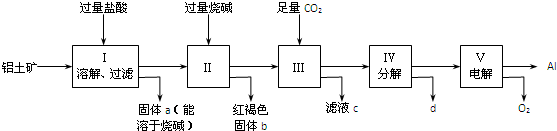
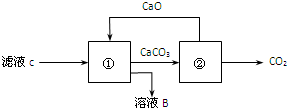
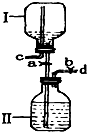 ��ͼ��ij�о���С����Ƶ�һ������װ��ͼ��
��ͼ��ij�о���С����Ƶ�һ������װ��ͼ��