题目内容
12.甲烷是一种理想的洁净燃料.已知:CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H=-802.3kJ•mol-1
H2O(1)═H2O(g),△H=+44.0kJ•mol-l 则甲烷的燃烧热为( )
| A. | 846.3 kJ•mol-l | B. | 758.3 kJ•mol-l | C. | 890.3 kJ•mol-l | D. | 714.3 kJ•mol-l |
分析 甲烷燃烧热中为1mol甲烷生成稳定氧化物时放出的热量,水为液态,以此来解答.
解答 解:由①CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-802.3kJ•mol-1
②H2O(1)═H2O(g)△H=+44.0kJ•mol-l,
结合盖斯定律可知,①-②×2得到CH4(g)+2O2(g)═CO2(g)+2H2O(l),其△H=(-802.3kJ•mol-1)-(+44.0kJ•mol-l)×2=-890.3 kJ•mol-l,
故选C.
点评 本题考查反应热与焓变,为高频考点,把握燃烧热、盖斯定律为解答的关键,侧重分析与应用能力的考查,注意盖斯定律的应用,题目难度不大.

练习册系列答案
 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案
相关题目
1.下列关于油脂的叙述正确的是( )
| A. | 油脂均为固体 | |
| B. | 油脂在体内直接氧化产生热量 | |
| C. | 多吃动物脂肪比多吃植物油有利 | |
| D. | 有些脂肪酸是人体必需的,但在人体内却不能合成;脂肪中必需脂肪酸的含量越高,其营养价值越高 |
3.化学与生产、生活、科技等密切相关,下列说法不正确的是( )
| A. | 加大清洁能源的开发利用,提髙资源的利用率 | |
| B. | 研发使用高效催化剂,可提高反应中原料的转化率 | |
| C. | 用K2FeO4取代Cl2处理饮用水,可杀菌消毒,还能沉降水中的悬浮物 | |
| D. | 用沼气、太阳能、风能等新型能源代替化石燃料 |
17.(Ⅰ)部分弱酸的电离平衡常数如表:
(1)室温下①0.1mol•L-1 HCOONa,②0.1mol•L-1 NaClO,③0.1mol•L-1 Na2CO3,④0.1mol•L-1 NaHCO3溶液的pH由大到小的关系为③②④①.
(2)浓度均为0.1mol•L-1的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为c(SO32-)>c(CO32-)>c(HCO3-)>c(HSO3-).
(3)少量CO2通入到过量的NaClO溶液中发生反应的离子方程式ClO-+CO2+H2O=HCO3-+HClO.
(4)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为c(HCOO-)>c(Na+)>c(H+)>c(OH-).
(Ⅱ)某小组运用工业上离子交换膜法制烧碱的原理,用如图所示装置电解K2SO4溶液.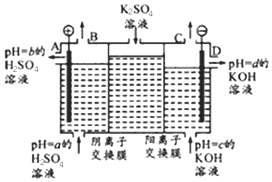
①该电解槽中通过阴离子交换膜的离子数<(填“>”“<”或“一”)通过阳离子交换膜的离子数;
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为b<a<c<d;
③电解一段时间后,B出口与C出口产生气体的质量比为8:1.
| 弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 电离平衡常数(25℃) | Ka=1.77 ×10-4 | Ka=4.0 ×10-8 | Ka1=4.3×10-7 Ka2=4.7×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
(2)浓度均为0.1mol•L-1的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为c(SO32-)>c(CO32-)>c(HCO3-)>c(HSO3-).
(3)少量CO2通入到过量的NaClO溶液中发生反应的离子方程式ClO-+CO2+H2O=HCO3-+HClO.
(4)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为c(HCOO-)>c(Na+)>c(H+)>c(OH-).
(Ⅱ)某小组运用工业上离子交换膜法制烧碱的原理,用如图所示装置电解K2SO4溶液.

①该电解槽中通过阴离子交换膜的离子数<(填“>”“<”或“一”)通过阳离子交换膜的离子数;
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为b<a<c<d;
③电解一段时间后,B出口与C出口产生气体的质量比为8:1.
4.下列实验现象描述正确的是( )
| A. | 红热的铜丝在硫蒸汽中燃烧,产生黑色固体 | |
| B. | 碘水中加入少量CCl4,振荡静置后,下层颜色变浅,上层颜色变为紫色 | |
| C. | 往溴水中加入碘化钠溶液,溴水变为无色 | |
| D. | 氢气在Cl2中燃烧产生白色的烟 |
1.加入Al能产生H2的溶液中一定能大量共存的是( )
| A. | K+、Na+、Br-、SO42- | B. | Na+、Ba2+、ClO-、Cl- | ||
| C. | Ca2+、Cl-、HCO3-、K+ | D. | NH4+、K+、OH-、SO42- |
2.用下列装置不能达到有关实验目的是( )
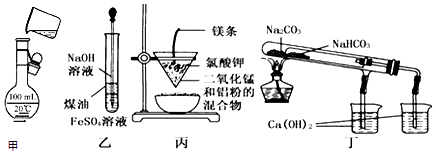

| A. | 用甲图所示装置将溶液定容到100 mL | |
| B. | 用乙图装置制备Fe(OH)2 | |
| C. | 用丙图装置可制得金属锰 | |
| D. | 用丁图装置验证NaHCO3和Na2CO3的热稳定性 |