题目内容
相同物质的量的 CO 和 CO2 相比较,下列叙述正确的是( )
①分子数之比为1:1
②所含氧原子数之比为1:2
③原子总数之比为2:3
④碳原子数之比为1:1
⑤电子数之比为7:11
⑥体积之比为1:1.
①分子数之比为1:1
②所含氧原子数之比为1:2
③原子总数之比为2:3
④碳原子数之比为1:1
⑤电子数之比为7:11
⑥体积之比为1:1.
| A、①③④ | B、②③④ |
| C、①②③④⑤ | D、①②③④⑤⑥ |
考点:阿伏加德罗定律及推论
专题:
分析:相同物质的量的 CO 和 CO2,
①分子数N=nNA;
②先计算其分子数之比,再根据分子构成计算O原子个数之比;
③先计算其分子数之比,再根据分子构成计算原子总数之比;
④先计算其分子数之比,再根据分子构成计算C原子个数之比;
⑤先计算其分子数之比,再根据分子构成计算电子总数之比;
⑥V=nVm.
①分子数N=nNA;
②先计算其分子数之比,再根据分子构成计算O原子个数之比;
③先计算其分子数之比,再根据分子构成计算原子总数之比;
④先计算其分子数之比,再根据分子构成计算C原子个数之比;
⑤先计算其分子数之比,再根据分子构成计算电子总数之比;
⑥V=nVm.
解答:
解:相同物质的量的 CO 和 CO2,
①根据N=nNA知,二者的分子数之比等于其物质的量之比,二者物质的量相等,所以其分子数相等,故正确;
②二者分子数相等,每个CO分子中含有1个O原子、每个二氧化碳分子中含有2个O原子,所以其O原子数之比为1:2,故正确;
③二者分子数相等,每个CO分子中含有2个原子、每个二氧化碳分子中含有3个原子,所以其原子总数之比为2:3,故正确;
④二者分子数相等,因为每个分子中C原子个数相等,所以其C原子总数相等,故正确;
⑤二者分子数相等,每个CO分子中含有14个电子、每个二氧化碳分子中电子数为22,所以其电子总数之比为7:11,故正确;
⑥温度和压强未知,所以气体摩尔体积未知,则无法计算其体积相对大小,故错误;
故选C.
①根据N=nNA知,二者的分子数之比等于其物质的量之比,二者物质的量相等,所以其分子数相等,故正确;
②二者分子数相等,每个CO分子中含有1个O原子、每个二氧化碳分子中含有2个O原子,所以其O原子数之比为1:2,故正确;
③二者分子数相等,每个CO分子中含有2个原子、每个二氧化碳分子中含有3个原子,所以其原子总数之比为2:3,故正确;
④二者分子数相等,因为每个分子中C原子个数相等,所以其C原子总数相等,故正确;
⑤二者分子数相等,每个CO分子中含有14个电子、每个二氧化碳分子中电子数为22,所以其电子总数之比为7:11,故正确;
⑥温度和压强未知,所以气体摩尔体积未知,则无法计算其体积相对大小,故错误;
故选C.
点评:本题考查阿伏伽德罗定律及其推论,明确物质的量公式中各个物理量的关系及分子构成是解本题关键,注意气体摩尔体积的适用范围及适用条件,题目难度不大.

练习册系列答案
相关题目
下列变化中,必须要加入氧化剂才能实现的是( )
| A、KMnO4→O2 |
| B、HCl→Cl2 |
| C、HCl→H2 |
| D、SO3→H2SO4 |
相对分子质量为M的某物质在室温下的溶解度为Sg水,此时测得饱和溶液的密度为dg/cm3,则该饱和溶液的物质的量浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
16g O2和16g O3相比,下列表述正确的是( )
| A、所含分子数相同 |
| B、16g O3中所含分子数较多 |
| C、所含原子数不同 |
| D、所含原子数相同 |
如图是实验室某硫酸试剂瓶标签上的部分内容,据此下列说法正确的是( )


| A、1 L该硫酸中氢原子的物质的量为36.8 mol |
| B、该硫酸与等体积的水混合所得溶液的质量分数小于49% |
| C、配制250.0 mL 4.6 mol/L的稀硫酸需取该硫酸62.5 mL |
| D、稀释该硫酸的方法是将水倒入盛该酸的量筒中 |
设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
| A、25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA |
| B、1 mol Cl2与足量Fe反应,转移的电子数为3NA |
| C、标准状况下,以任意比混合的氢气和一氧化碳气体共8.96 L,在足量氧气中充分燃烧时消耗氧气的分子数为0.2NA |
| D、7.1 g Cl2与足量的NaOH溶液反应转移的电子数约为0.2 NA |
下列说法正确的是( )
| A、CCl4曾用作灭火剂,但因与水在高温下反应会产生有毒物质,现已被禁用 |
| B、蔗糖、油脂及它们的水解产物均为非电解质 |
| C、棉花、羊毛、腈纶和涤纶都属于合成纤维 |
| D、将纳米材料分散到液体分散剂中,该分散系可发生丁达尔现象,可推测纳米材料的直径为1~100nm之间 |
YBa2Cu8Ox(Y为元素钇)是一种重要的超导材料,下列关于
Y的说法错误的是( )
89 39 |
| A、属于金属元素 | ||||
| B、质子数与中子数之差为50 | ||||
| C、原子的核外电子数是39 | ||||
D、
|
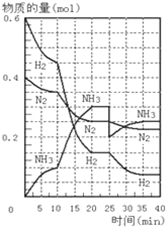 500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应:3H2+N2?2NH3△H<0.反应过程中H2、N2和NH3物质的量变化如图所示,据图判断下列叙述不正确的是( )
500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应:3H2+N2?2NH3△H<0.反应过程中H2、N2和NH3物质的量变化如图所示,据图判断下列叙述不正确的是( )| A、反应开始到第一次平衡时,N2的平均反应速率为0.0625mol?(L?min)-1,H2的转化率为75% |
| B、反应达到第一次平衡时,反应的平衡常数表达式可写作:K=c2(NH3)/[c3(H2)?c(N2)]=(0.15 mol?L-1)2/[(0.075 mol?L-1)3?(0.125 mol?L-1)] |
| C、从曲线变化可以看出,反应进行到10min至20min时可能采取的措施是使用了催化剂 |
| D、从曲线变化可以看出,反应进行至25min时,采取的措施是分离出0.1mol的氨气,平衡正向移动 |