题目内容
9.下列各组物质中,所含分子数一定相同的是( )| A. | 1 g H2和8 g O2 | |
| B. | 常温常压下,28 g CO和6.02×1022个CO分子 | |
| C. | 0.1 mol HCl和2.24 L He | |
| D. | 150℃、1.01×105 Pa时,18 L H2O和18 L CO2 |
分析 A.依据N=$\frac{m}{M}$×NA计算解答;
B.依据N=$\frac{m}{M}$×6.02×1023mol-1计算;
C.气体状况未知;
D.同温同压下,相同体积的气体具有相同分子数.
解答 解:A.1 g H2分子数为$\frac{1g}{2g/mol}$×NA=0.5NA,8 g O2分子数为$\frac{8g}{32g/mol}$×NA=0.25NA,二者分子数不相等,故A错误;
B.28 g CO含有分子数为;$\frac{28g}{28g/mol}$×6.02×1023mol-1=6.02×1023,与6.02×1022个CO分子数不相等,故B错误;
C.气体状况未知,无法计算He的物质的量和分子数,故C错误;
D.150℃、1.01×105 Pa时,水与二氧化碳都是气体,二者体积相同,则具有相同的分子数,故D正确;
故选:D.
点评 本题考查了物质所含微粒个数大小比较,明确以物质的量为核心计算公式是解题关键,题目难度不大.

练习册系列答案
相关题目
14.完全中和10mLpH=13的Ba(OH)2 溶液,需要0.10mol/L 的盐酸( )
| A. | 5mL | B. | 10mL | C. | 15mL | D. | 20mL |
20.如表所示,为提纯下列物质(括号内为少量杂质),所选用的除杂试剂与主要分离方法都正确的是( )
| 不纯物质 | 除杂试荆 | 分离方法 | |
| A | NH4Cl溶液(AlCl3) | NaOH溶液 | 过滤 |
| B | 蛋白质溶液(NaCl) | 蒸馏水 | 渗析 |
| C | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| D | 四氯化碳(I2) | NaOH溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
17.下列物质属于纯净物的是( )
| A. | 玻璃 | B. | 纤维素 | C. | 天然油脂 | D. | 冰水混合物 |
4.将0.2mol•L-1的HCN溶液和0.1mol•L-1的NaOH溶液等体积混合后,溶液显碱性,下列关系式中正确的是( )
| A. | c(HCN)<c(CN-) | B. | c(Na+)>c(CN-) | ||
| C. | c(HCN)-c(CN-)=c(OH-) | D. | c(HCN)+c(CN-)=0.2mol•L-1 |
14.一定量的锌粒与足量稀硫酸反应,向反应混合液中加入某些物质,下列判断正确的是( )
| A. | 加入少量水,产生H2速率减小,H2体积不变 | |
| B. | 加入NH4HSO4固体,产生H2速率不变,H2体积不变 | |
| C. | 加入CH3COONa固体,产生H2速率减小,H2体积减小 | |
| D. | 滴加少量CuSO4溶液,产生H2速率变大,H2体积不变 |
1.下列离子方程式书写不正确的是( )
| A. | 将H2S气体通入Fecl3溶液中:H2S+2Fe3+=2Fe2++S↓+2H+ | |
| B. | Si与NaOH溶液反应:Si+2OH-+H2O=SiO32-+2H2↑ | |
| C. | 将Cl2和SO2体积比1:1同时通入水中:Cl2+SO2+2H2O=4H++SO42-+2Cl- | |
| D. | 将CO2气体通入饱和Na2CO3溶液中:CO2+H2O+CO32-=2HCO3- |
19.将纯锌片和纯铜片按图示方式插入同浓度同体积的稀硫酸中 一段时间,以下叙述正确的是( )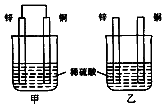

| A. | 两烧杯中铜片表面均无气泡产生 | |
| B. | 两烧杯中溶液的pH均增大 | |
| C. | 甲中电子通过导线由锌片流向铜片,再回到锌片 | |
| D. | 乙中产生气泡的速度比甲快 |
