题目内容
NaHCO3和Na2CO3?xH2O的混合物,为了测定x值,某同学采用如图所示的装置进行实验(CaCl2、碱石灰均足量).
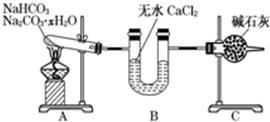
(1)A装置的作用是 .
(2)B装置的作用是 .
(3)C装置的作用是 .
(4)若在装置A的试管中装入NaHCO3和Na2CO3?xH2O的混合物3.7g,用酒精灯加热到反应完全,此时B管增重1.89g,C管增重0.22g,则x的值为 .
(5)该装置还不是很完善,可能使测定结果偏小,应如何改进 .为什么? .

(1)A装置的作用是
(2)B装置的作用是
(3)C装置的作用是
(4)若在装置A的试管中装入NaHCO3和Na2CO3?xH2O的混合物3.7g,用酒精灯加热到反应完全,此时B管增重1.89g,C管增重0.22g,则x的值为
(5)该装置还不是很完善,可能使测定结果偏小,应如何改进
考点:探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:(1)在加热的条件下碳酸氢钠易分解生成碳酸钠、水和CO2,而碳酸钠晶体也易失去结晶水,所以A装置的作用是加热,使NaHCO3分解,使Na2CO3?H2O失水;
(2)无水氯化钙能吸收水蒸气,通过称量反应前后的质量可以得出水蒸气的质量,因此B装置的作用是吸收反应中生成的水;
(3)由于反应中还有CO2生成,而碱石灰可以吸收CO2,因此通过称量反应前后的质量,可以得出CO2的质量,所以C装置的作用是吸收反应中生成的CO2;
(4)用酒精灯加热到反应完全,此时B管增重1.89g,C管增重0.22 g,这说明反应中生成的水蒸气质量=1.89g,CO2质量=0.22g,物质的量分别是
=0.105mol、
=0.005mol.根据反应的方程式2NaHCO3
Na2CO3+H2O+CO2↑可知,该反应中生成的CO2就是0.005mol,则碳酸氢钠的物质的量是0.005mol×2=0.01mol,反应中生成的水是0.005mol.则碳酸钠在反应中失去的水的物质的量=0.105mol-0.005mol=0.100mol.碳酸氢钠的质量=0.01mol×84g/mol=0.84g,计算得到碳酸钠质量分数;
(5)由于空气中也含有CO2和水蒸气,也能被C装置的中碱石灰吸收,从而导致C管增重偏高,因此测量值偏低;所以改进的措施为在C装置后再加一个装有碱石灰的U形管;为了防止空气中的CO2和H2O被C装置的中的碱石灰吸收.
(2)无水氯化钙能吸收水蒸气,通过称量反应前后的质量可以得出水蒸气的质量,因此B装置的作用是吸收反应中生成的水;
(3)由于反应中还有CO2生成,而碱石灰可以吸收CO2,因此通过称量反应前后的质量,可以得出CO2的质量,所以C装置的作用是吸收反应中生成的CO2;
(4)用酒精灯加热到反应完全,此时B管增重1.89g,C管增重0.22 g,这说明反应中生成的水蒸气质量=1.89g,CO2质量=0.22g,物质的量分别是
| 1.89g |
| 18g/mol |
| 0.22g |
| 44g/mol |
| ||
(5)由于空气中也含有CO2和水蒸气,也能被C装置的中碱石灰吸收,从而导致C管增重偏高,因此测量值偏低;所以改进的措施为在C装置后再加一个装有碱石灰的U形管;为了防止空气中的CO2和H2O被C装置的中的碱石灰吸收.
解答:
解:(1)在加热的条件下碳酸氢钠易分解生成碳酸钠、水和CO2,而碳酸钠晶体也易失去结晶水,所以A装置的作用是加热,使NaHCO3分解,使Na2CO3?H2O失水;
故答案为:使NaHCO3分解,使Na2CO3?H2O失水;
(2)无水氯化钙能吸收水蒸气,通过称量反应前后的质量可以得出水蒸气的质量,因此B装置的作用是吸收反应中生成的水;
故答案为:吸收反应中生成的水;
(3)由于反应中还有CO2生成,而碱石灰可以吸收CO2,因此通过称量反应前后的质量,可以得出CO2的质量,所以C装置的作用是吸收反应中生成的CO2;
故答案为:吸收反应中生成的CO2;
(4)用酒精灯加热到反应完全,此时B管增重1.89g,C管增重0.22 g,这说明反应中生成的水蒸气质量=1.89g,CO2质量=0.22g,物质的量分别是
=0.105mol、
=0.005mol.根据反应的方程式2NaHCO3
Na2CO3+H2O+CO2↑可知,该反应中生成的CO2就是0.005mol,则碳酸氢钠的物质的量是0.005mol×2=0.01mol,反应中生成的水是0.005mol.则碳酸钠在反应中失去的水的物质的量=0.105mol-0.005mol=0.100mol.碳酸氢钠的质量=0.01mol×84g/mol=0.84g,则样品中碳酸钠晶体的质量=3.7g-0.84g=2.86g.则
×x=0.1mol,解得x=10;
故答案为:10;
(5)由于空气中也含有CO2和水蒸气,也能被C装置的中碱石灰吸收,从而导致C管增重偏高,因此测量值偏低;所以改进的措施为在C装置后再加一个装有碱石灰的U形管;为了防止空气中的CO2和H2O被C装置的中的碱石灰吸收;
故答案为:在C装置后再加一个装有碱石灰的U形管;为了防止空气中的CO2和H2O被C装置的中的碱石灰吸收;
故答案为:使NaHCO3分解,使Na2CO3?H2O失水;
(2)无水氯化钙能吸收水蒸气,通过称量反应前后的质量可以得出水蒸气的质量,因此B装置的作用是吸收反应中生成的水;
故答案为:吸收反应中生成的水;
(3)由于反应中还有CO2生成,而碱石灰可以吸收CO2,因此通过称量反应前后的质量,可以得出CO2的质量,所以C装置的作用是吸收反应中生成的CO2;
故答案为:吸收反应中生成的CO2;
(4)用酒精灯加热到反应完全,此时B管增重1.89g,C管增重0.22 g,这说明反应中生成的水蒸气质量=1.89g,CO2质量=0.22g,物质的量分别是
| 1.89g |
| 18g/mol |
| 0.22g |
| 44g/mol |
| ||
| 2.86g |
| (106+18x)g/mol |
故答案为:10;
(5)由于空气中也含有CO2和水蒸气,也能被C装置的中碱石灰吸收,从而导致C管增重偏高,因此测量值偏低;所以改进的措施为在C装置后再加一个装有碱石灰的U形管;为了防止空气中的CO2和H2O被C装置的中的碱石灰吸收;
故答案为:在C装置后再加一个装有碱石灰的U形管;为了防止空气中的CO2和H2O被C装置的中的碱石灰吸收;
点评:本题考查了物质组成的实验探究和实验测定方法分析,质量分数计算应用,掌握实验基本操作和物质性质是关键,题目难度中等.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
下列说法正确的是( )
| A、需要加热方能发生的反应一定是吸热反应 |
| B、放热的反应在常温下一定很易发生 |
| C、一个反应是放热反应还是吸热反应主要由反应物、生成物所具有的总能量的相对大小决定,而不是由反应是否需要加热而决定 |
| D、吸热反应发生过程中要不断从外界获得能量、放热反应发生过程中不再需要外界能量 |
依据下列实验,不能证明一元酸HR是弱酸的是( )
| A、室温下NaR溶液的pH大于7 |
| B、加热NaR溶液时,溶液的pH变小 |
| C、稀盐酸中加入少量NaR固体,溶解后溶液的pH变大 |
| D、HR溶液中加少量NaR固体,溶解后溶液的pH变大 |