题目内容
下列书写或说法正确的是( )
| A、聚丙烯的链节是-CH2-CH2-CH2- | |||
B、向苯酚溶液中滴加Na2CO3溶液: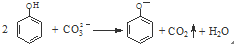 | |||
C、CH3COOH+CH3CH218OH
| |||
| D、苯的同系物能使酸性高锰酸钾溶液褪色,说明烃基对苯环的性质产生了较大的影响 |
考点:离子方程式的书写,苯的同系物的化学性质,乙酸的酯化反应
专题:
分析:A.聚丙烯的链节是-CH2-CH(CH3)-;
B.苯酚酸性小于碳酸,苯酚与碳酸钠溶液反应生成碳酸氢钠,不会生成二氧化碳;
C.酯化反应原理为酸脱羟基醇脱氢,所以乙醇的18O原子反应后包含在乙酸乙酯中;
D.苯的同系物能使酸性高锰酸钾溶液褪色,被氧化的是苯的同系物的侧链C,是苯环对侧链的影响.
B.苯酚酸性小于碳酸,苯酚与碳酸钠溶液反应生成碳酸氢钠,不会生成二氧化碳;
C.酯化反应原理为酸脱羟基醇脱氢,所以乙醇的18O原子反应后包含在乙酸乙酯中;
D.苯的同系物能使酸性高锰酸钾溶液褪色,被氧化的是苯的同系物的侧链C,是苯环对侧链的影响.
解答:
解:A.聚丙烯的结构简式为: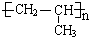 ,聚丙烯的链节为:-CH2-CH(CH3)-,故A错误;
,聚丙烯的链节为:-CH2-CH(CH3)-,故A错误;
B.苯酚与碳酸钠溶液反应生成碳酸氢钠、苯酚钠,正确的离子方程式为: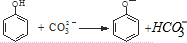 ,故B错误;
,故B错误;
C.CH3COOH和CH3CH218OH发生酯化反应的化学方程式为:CH3COOH+CH3CH218OH
CH3CO18OCH2CH3+H2O,故C正确;
D.苯的同系物能使酸性高锰酸钾溶液褪色,被氧化的是苯的同系物的侧链C原子,应该为苯环对侧链的影响,导致侧链碳原子变得比较活泼,故D错误;
故选C.
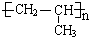 ,聚丙烯的链节为:-CH2-CH(CH3)-,故A错误;
,聚丙烯的链节为:-CH2-CH(CH3)-,故A错误;B.苯酚与碳酸钠溶液反应生成碳酸氢钠、苯酚钠,正确的离子方程式为:
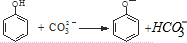 ,故B错误;
,故B错误;C.CH3COOH和CH3CH218OH发生酯化反应的化学方程式为:CH3COOH+CH3CH218OH
| 浓H2SO4 |
| △ |
D.苯的同系物能使酸性高锰酸钾溶液褪色,被氧化的是苯的同系物的侧链C原子,应该为苯环对侧链的影响,导致侧链碳原子变得比较活泼,故D错误;
故选C.
点评:本题考查了离子方程式、化学方程式的正误判断,题目难度中等,注意掌握化学方程式、离子方程式的书写原则,明确常见有机物结构与性质,试题知识点较多、综合性较强,充分考查了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
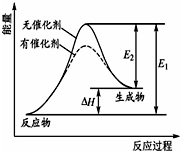 某反应的过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
某反应的过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A、该反应为放热反应 |
| B、催化剂能改变反应的焓变 |
| C、催化剂能降低反应的活化能E1和 E2 |
| D、增大反应物的浓度,可使单位体积内活化分子百分数增大,反应速率加快 |
下列物质中有自由移动的氯离子的是( )
| A、氯化钠晶体 |
| B、熔化的氯化钾 |
| C、氯酸钾溶液 |
| D、液态氯化氢 |
氮化铝具有耐高温、抗冲击、导热性好等优良性质,广泛应用于电子工业、陶瓷工业等领域.在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C═2AlN+3CO,下列说法正确的是( )
| A、该反应为不属于氧化还原反应 |
| B、Al2O3是氧化剂 |
| C、每生成2mol AlN转移6 mol电子 |
| D、C发生还原反应 |
下列电离方程式错误的是( )
| A、Na2CO3═2Na++CO32- |
| B、NaHCO3═Na++HCO3- |
| C、H2SO4═2H++SO42- |
| D、KClO3═K++Cl-+3O2- |
下列离子方程式书写正确的是( )
| A、铜与稀硝酸的反应:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
| B、氯气与水反应:Cl2+H2O=H++Cl-+HClO |
| C、铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| D、钠和水反应:2Na+H2O=2Na++2OH-+H2↑ |
下列说法正确的是(NA表示阿伏加德罗常数)( )
| A、在常温常压下,11.2 升氯气含有的分子数为0.5NA |
| B、在常温常压下,1摩尔气体含有的原子数为NA |
| C、32 g氧气所含原子数目为2NA |
| D、在同温同压下,相同体积的任何气体单质所含原子数目相同 |
下列说法正确的是( )
| A、红磷转化为白磷是化学变化 |
| B、原子是不能再分的最小微粒 |
| C、O3是由3个氧原子构成的化合物 |
| D、冰水混合物属于混合物 |