题目内容
【化学——选修3:物质结构与性质】(15分)
氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解。
(1) COCl2的空间构型为 ;溴的价电子排布式为 。
(2)已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列 式发生。
A. CsICl2=CsCl+ICl B. CsICl2=CsI+Cl2
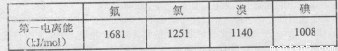
(3)根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是 。
(4)下列分子既不存在s-p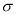 键,也不存在p-p
键,也不存在p-p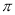 键的是 。
键的是 。
A. HCl B.HF C.SO2 D.SCl2
(5)已知ClO2一为角型,中心氯原子周围有四对价层电子。ClO2-中心氯原子的杂化轨道类型为
,写出CN-的等电子体的分子式 (写出1个)。
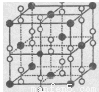
(6)钙在氧气中燃烧时得到一种钙的氧化物品体,其结构如图所示:由此可判断该钙的氧化物的化学式为____ 。已知该氧化物的密度是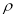 g·cm-3,则晶胞离得最近的两个钙离子间的距离为____ cm(只要求列算式,不必计算出数值,阿伏加德罗常数为NA)。
g·cm-3,则晶胞离得最近的两个钙离子间的距离为____ cm(只要求列算式,不必计算出数值,阿伏加德罗常数为NA)。
(1)平面形(1分);4s24p5(1分);(2)A(1分);(3)碘(2分);
(4)D(2分);(5)sp3杂化(2分);N2 或 CO(2分)
(6)CaO2 (2分)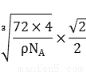 (2分)。
(2分)。
【解析】
试题分析:(1) COCl2的空间构型为平面形,35号元素溴最外层有7个电子,其价电子排布式为4s24p5;(2)因为CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,按照A方式分解产生的CsCl的晶格能大于按照B方式分解产生的CsI的晶格能,所以分解发生是A;(3)第一电离能越小,元素的原子越容易失去电子,则形成单核阳离子,根据表格的数据可知选项应该是碘元素;(4)A.HCl存在s-p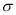 键,错误;B.HF s-p
键,错误;B.HF s-p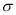 键,错误;C.SO2存在p-p
键,错误;C.SO2存在p-p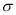 键和p-p
键和p-p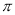 键,错误;D.SCl2存在p-p
键,错误;D.SCl2存在p-p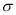 键,不存在s-p
键,不存在s-p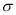 键,和p-p
键,和p-p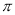 键,正确。(5)已知ClO2一为角型,中心氯原子周围有四对价层电子。ClO2-中心氯原子的杂化轨道类型为sp3杂化;等电子体是微粒中的原子个数相等,最外层电子数也相等的物质。与CN-的等电子体的分子式N2 或 CO;(6)根据晶胞结构可知在一个晶胞中含有Ca:8×1/8+6×1/2=4;含有的O原子个数是:12×2×1/4+2=8,所以该钙的氧化物的化学式为CaO2;每个晶胞中含有4个CaO2。根据晶胞结构可知在晶胞离得最近的两个钙离子间的距离为面对角线的一半。假设晶胞的边长是L,则
键,正确。(5)已知ClO2一为角型,中心氯原子周围有四对价层电子。ClO2-中心氯原子的杂化轨道类型为sp3杂化;等电子体是微粒中的原子个数相等,最外层电子数也相等的物质。与CN-的等电子体的分子式N2 或 CO;(6)根据晶胞结构可知在一个晶胞中含有Ca:8×1/8+6×1/2=4;含有的O原子个数是:12×2×1/4+2=8,所以该钙的氧化物的化学式为CaO2;每个晶胞中含有4个CaO2。根据晶胞结构可知在晶胞离得最近的两个钙离子间的距离为面对角线的一半。假设晶胞的边长是L,则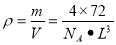 ;
;
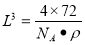 .L=
.L= ,所以晶胞离得最近的两个钙离子间的距离为
,所以晶胞离得最近的两个钙离子间的距离为 。
。
考点:考查原子的价电子排布式、物质的分子结构、晶体结构、晶体化学式的确定、物质晶体中微粒之间的距离的计算的知识。

 口算题天天练系列答案
口算题天天练系列答案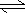 H++HA-,HA-
H++HA-,HA-  H++A2-
H++A2-

 、SO
、SO
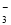 、Na+
、Na+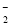 、NO
、NO 、K+
、K+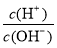 =1012的溶液中:NH
=1012的溶液中:NH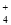 、Al3+、NO
、Al3+、NO