题目内容
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,22.4L氧气做氧化剂时转移的电子数一定是4NA |
| B、1mol硝基(-NO2)与NA个二氧化氮(NO2)分子所含的电子数相等 |
| C、80 mL 12 mol/L的浓盐酸与足量MnO2反应,生成的Cl2分子数目为0.24NA |
| D、氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24L |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.氧气与钠的反应中,1mol氧气完全反应转移了2mol电子;
B.硝基和二氧化氮中都含有23个电子,物质的量相等时含有的电子数相等;
C.二氧化锰与浓盐酸的反应中,随着反应的进行,浓盐酸变成稀盐酸,反应停止,反应生成氯气的物质的量减小;
D.不是标准状况下,不能使用标况下的气体摩尔体积计算混合气体的体积.
B.硝基和二氧化氮中都含有23个电子,物质的量相等时含有的电子数相等;
C.二氧化锰与浓盐酸的反应中,随着反应的进行,浓盐酸变成稀盐酸,反应停止,反应生成氯气的物质的量减小;
D.不是标准状况下,不能使用标况下的气体摩尔体积计算混合气体的体积.
解答:
解:A.标况下22.4L氧气的物质的量为1mol,1mol氧气与钠反应生成1mol过氧化钠,转移了2mol电子,转移的电子为2NA,故A错误;
B.1mol硝基(-NO2)中含有23个电子,NA个二氧化氮的物质的量为1mol,1molNO2分子含有23mol电子,二者所含的电子数相等,故B正确;
C.80mL mL 12 mol/L的浓盐酸中含有0.96mol氯化氢,浓盐酸与二氧化锰的反应中,消耗0.96mol氯化氢会生成0.24mol氯气,由于随着反应的进行,浓盐酸会变成稀盐酸,反应停止,则反应生成的氯气小于0.24mol,生成的Cl2分子数目小于0.24NA,故C错误;
D.没有告诉在标况下,题中条件无法计算混合气体的体积,故D错误;
故选B.
B.1mol硝基(-NO2)中含有23个电子,NA个二氧化氮的物质的量为1mol,1molNO2分子含有23mol电子,二者所含的电子数相等,故B正确;
C.80mL mL 12 mol/L的浓盐酸中含有0.96mol氯化氢,浓盐酸与二氧化锰的反应中,消耗0.96mol氯化氢会生成0.24mol氯气,由于随着反应的进行,浓盐酸会变成稀盐酸,反应停止,则反应生成的氯气小于0.24mol,生成的Cl2分子数目小于0.24NA,故C错误;
D.没有告诉在标况下,题中条件无法计算混合气体的体积,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确二氧化氮与硝基、羟基与氢氧根离子的区别,选项C为易错点,注意稀盐酸不与二氧化锰反应.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列观点正确的是( )
| A、相对分子质量相同,必定同一种物质或同分异构体 |
| B、乙酸乙酯、油脂与NaOH溶液反应均有乙醇生成 |
| C、用溴水即可鉴别苯酚溶液、2,4-已二烯和甲苯 |
| D、分子式相差一个或若干个“CH2”的有机物必定属于同系物 |
常温下,下列说法正确的是( )
| A、往CH3COOH溶液中加水,c(OH-)和c(H+)均增大 |
| B、物质的量浓度均为0.1mol?1-1的CH3COOH溶液和NaOH溶液等体积混合,c(Na+)>(CH3COO-) |
| C、某浓度的氯化铵溶液中存在c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| D、在pH=4的氯化铵溶液中c(H+)+c(NH4+)=c(Cl-)+c(OH-) |
下列叙述正确的是( )
| A、1 mol H2O的质量为18g/mol |
| B、CH4的摩尔质量为16g |
| C、3.01×1023个SO2分子的质量为32g |
| D、摩尔是国际单位制中的一个基本物理量 |
对下列有机反应类型的判断中不正确的是( )
A、CH3CH2OH+CH3COOH
| |||
B、CH2=CH2+HOCl
| |||
C、2CH3CH2OH+O2
| |||
D、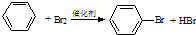 加成反应 加成反应 |
下列实验操作中正确的是( )
| A、配制一定物质的量浓度的硫酸溶液时,用量筒量取一定体积的浓硫酸倒入烧杯后,再用蒸馏水洗涤量筒2~3次,并将洗涤液一并倒入烧杯中稀释 |
| B、倒入漏斗的过滤液的液面应低于滤纸边缘 |
| C、用胶头滴管向试管中加入液体时,为防止滴在试管外面,应将滴管尖嘴处伸入试管口中 |
| D、称量氢氧化钠固体的质量时,将称量物放在纸片上,并置于托盘天平的左盘,砝码放在托盘天平的右盘 |
下列物质的酸性强弱比较正确的是( )
| A、HBrO4<HIO4 |
| B、H2SO4<H3PO4 |
| C、HClO3<HClO |
| D、H2SO4>H2SO3 |
在反应2KClO3═2KCl+3O2↑中,电子转移的总数是( )
| A、2个 | B、6个 | C、12个 | D、5个 |
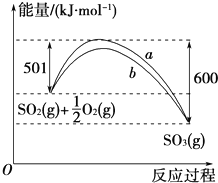 根据下列叙述写出相应的热化学方程式:
根据下列叙述写出相应的热化学方程式: