题目内容
7.某气态烃A与H2的相对密度为14,其产量可以用来衡量一个国家的石油化工发展水平.以该化合物为原料合成化合物G、E和I的流程如下:已知:Ⅰ.芳香族化合物F为C、H、O化合物,其相对分子质量为166,环上的一氯代物有一种,1mol F与足量NaHCO3溶液反应能生成2mol CO2,F与足量B反应生成G.
Ⅱ.H为二元醇,其蒸气密度折算成标准状况为2.77g/L,H与足量D反应生成I.
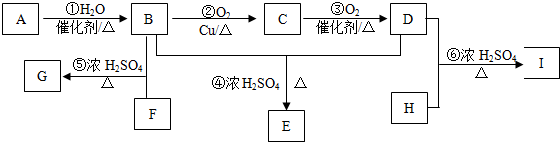
(1)A中官能团的名称为碳碳双键,E的结构简式CH3COOCH2CH3.
(2)G的分子式为C12H14O4,反应⑤的反应类型为酯化反应或取代反应.
(3)写出下列化学方程式:
②2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O;
⑥2CH3COOH+HOCH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2OOCCH3+2H2O.
分析 某气态烃A与H2的相对密度为14,该气体的相对分子质量为28,其产量可以用来衡量一个国家的石油化工发展水平,则A为CH2=CH2,乙烯与水发生加成反应生成B为CH3CH2OH,乙醇发生催化氧化生成C为CH3CHO,C进一步发生氧化反应生成D为CH3COOH,乙酸与乙醇发生酯化反应生成E为CH3COOCH2CH3;芳香族化合物F为C、H、O化合物,1mol F与足量NaHCO3溶液反应能生成2mol CO2,则F含有2个羧基,其相对分子质量为166,2个羧基、1个C6H4的总式量为45×2+(12×6+4)=166,则F含有1个苯环、2个羧基,且环上的一氯代物有一种,则F为 ,F与足量的B发生酯化反应生成G为
,F与足量的B发生酯化反应生成G为 ,H为二元醇,其蒸气密度折算成标准状况为2.77g/L,其相对分子质量为22.4×2.77=62,去掉2个羟基剩余基团式量为62-17×2=28,故为-C2H4-,则H为HOCH2CH2OH,H与足量D反应生成I为
,H为二元醇,其蒸气密度折算成标准状况为2.77g/L,其相对分子质量为22.4×2.77=62,去掉2个羟基剩余基团式量为62-17×2=28,故为-C2H4-,则H为HOCH2CH2OH,H与足量D反应生成I为 ,据此解答.
,据此解答.
解答 解:某气态烃A与H2的相对密度为14,该气体的相对分子质量为28,其产量可以用来衡量一个国家的石油化工发展水平,则A为CH2=CH2,乙烯与水发生加成反应生成B为CH3CH2OH,乙醇发生催化氧化生成C为CH3CHO,C进一步发生氧化反应生成D为CH3COOH,乙酸与乙醇发生酯化反应生成E为CH3COOCH2CH3;芳香族化合物F为C、H、O化合物,1mol F与足量NaHCO3溶液反应能生成2mol CO2,则F含有2个羧基,其相对分子质量为166,2个羧基、1个C6H4的总式量为45×2+(12×6+4)=166,则F含有1个苯环、2个羧基,且环上的一氯代物有一种,则F为 ,F与足量的B发生酯化反应生成G为
,F与足量的B发生酯化反应生成G为 ,H为二元醇,其蒸气密度折算成标准状况为2.77g/L,其相对分子质量为22.4×2.77=62,去掉2个羟基剩余基团式量为62-17×2=28,故为-C2H4-,则H为HOCH2CH2OH,H与足量D反应生成I为
,H为二元醇,其蒸气密度折算成标准状况为2.77g/L,其相对分子质量为22.4×2.77=62,去掉2个羟基剩余基团式量为62-17×2=28,故为-C2H4-,则H为HOCH2CH2OH,H与足量D反应生成I为 ,
,
(1)A是乙烯,A中官能团的名称为碳碳双键,E的结构简式CH3COOCH2CH3,
故答案为:碳碳双键;CH3COOCH2CH3;
(2)G为 ,其分子式为C12H14O4,反应⑤的反应类型为酯化反应或取代反应;
,其分子式为C12H14O4,反应⑤的反应类型为酯化反应或取代反应;
故答案为:C12H14O4;酯化反应或取代反应;
(3)②为乙醇的催化氧化,反应方程式为2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O;
反应⑥的化学方程式为:2CH3COOH+HOCH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2OOCCH3+2H2O,
故答案为:2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O;2CH3COOH+HOCH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2OOCCH3+2H2O.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断及获取信息解答问题能力,明确有机物官能团及其性质关系、物质之间的转化等知识点是解本题关键,注意抓住题干中信息分析解答,题目难度不大.

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案| A. | 等于20 mL | B. | 等于30 mL | C. | 大于30 mL | D. | 小于20 mL |
| A. | CuO与H2的反应在表面皿上进行 | |
| B. | 蒸发NaC1溶液得到NaCl晶体用蒸发皿 | |
| C. | 加热CuSO4•5H2O获得CuSO4用坩埚 | |
| D. | 盐酸与金属Mg的反应可在试管中进行 |
| A. | 以石墨作电极电解饱和氯化钠溶液:2Cl-+2H2O$\stackrel{电解}{→}$ 2OH-+H2↑+Cl2↑ | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+→Fe3++3H2O | |
| C. | H218O中投入少量Na2O2固体:2H218O+2O22-→4OH-+18O2↑ | |
| D. | CuCl2溶液中加入NaHS溶液:Cu2++HS-→CuS↓+H+ |
| A. | 金刚石 | B. | 石墨 | C. | CO | D. | C60 |
| A. | 还原性:K>Na>Mg | B. | 氢化物的稳定性:H2O<H2S<H2Se | ||
| C. | 酸性:H3PO4<H2SO4<HCl | D. | 原子半径:Na<Mg<Al |

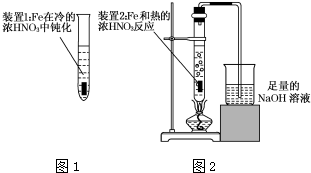 Fe、Cu都是人类较早使用的金属,某校化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质.请你参与研究并回答下列问题:
Fe、Cu都是人类较早使用的金属,某校化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质.请你参与研究并回答下列问题: