题目内容
15.在2L密闭容器中进行反应:mX(g)+nY(g)?pZ(g)+qQ(g),式中m、n、p、q为化学计量数.在0~3min内,各物质物质的量的变化如表所示:| 物质 | X | Y | Z | Q |
| 时间 | ||||
| 起始/mol | 0.7 | 1 | ||
| 2min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
| 3min末/mol | 0.8 |
(1)2min内Z的反应速率v(Z)=0.05mol•L-1•min-1.
(2)试确定以下物质的相关量:起始时n(Y)=2.3mol,n(Q)=3mol.
(3)方程式中m=1,n=4,p=2,q=3.
(4)对于该反应,能增大正反应速率的措施是CD
A.增大容器体积 B.移走部分Q C.通入大量X D.升高温度.
分析 (1)2min内Z的反应速率v(Z)=$\frac{\frac{△n}{V}}{△t}$;
(2)根据Z的反应速率计算Y的反应速率,根据△n=v△tV计算Y、Q参加反应的物质的量,从而确定反应开始n(Y)、n(Q);
(3)计算X的平均反应速率,同一可逆反应同一时间段内各物质的反应速率之比等于其计量数之比;
(4)增大反应物浓度、升高温度、增大压强、加入催化剂等方法都能正反应速率.
解答 解:(1)2min内Z的反应速率v(Z)=$\frac{\frac{△n}{V}}{△t}$=$\frac{\frac{1-0.8}{2}}{2}$mol•L-1•min-1=0.05 mol•L-1•min-1,
故答案为:0.05 mol•L-1•min-1;
(2)v(Z):v(Y)=1:2,则v(Y)=2v(Z)=2×0.05 mol•L-1•min-1=0.1 mol•L-1•min-1,
参加反应的△n(Y)=v(Y)△tV=0.1mol/(L.min)×2L×2min=0.4mol,则反应初始n(Y)=2.7mol-0.4mol=2.3mol
2min内v(Q)=0.075mol•L-1•min-1,参加反应的△n(Q)=v(Q)△tV=0.075mol/(L.min)×2L×2min=0.3mol,则反应初始n(Q)=2.7mol+0.3mol=3mol;
故答案为:2.3 mol;3 mol;
(3)v(X)=$\frac{\frac{0.8-0.7}{2}}{2}$mol/(L.min)=0.025mol/(L.min),同一可逆反应中同一段时间内各物质的反应速率之比等于其计量数之比,所以m:n:p:q=0.025mol/(L.min):0.1 mol•L-1•min-1:0.05 mol•L-1•min-1:0.075mol•L-1•min-1=1:4:2:3,
故答案为:1;4;2;3;
(4)增大反应物浓度、升高温度、增大压强、加入催化剂等方法都能正反应速率,所以符合条件的只有CD,故答案为:C D.
点评 本题考查化学平衡计算及外界条件对化学反应速率影响,为高频考点,侧重考查学生分析判断及计算能力,熟练掌握化学反应速率计算有关公式,题目难度不大.

①c(H+)②n(H+) ③$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$④$\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$⑤c(OH-) ⑥c(CH3COO-)
| A. | ①②③ | B. | ②③⑤ | C. | ④⑤ | D. | ④⑤⑥ |
| 容量 | 甲 | 乙 | 丙 | 丁 |
| A | 2mol | 1mol | 2mol | 1mol |
| B | 1mol | 1mol | 2mol | 2mol |
| A. | A的转化率:丁>丙>乙>甲 | B. | A的转化率:丁>乙>丙>甲 | ||
| C. | B的转化率:丙>甲>乙>丁 | D. | B的转化率:甲>乙>丙>丁 |
| 甲 | 乙 | 丙 | 丁 | ||
| 密闭容器体积/L | 2 | 2 | 2 | 1 | |
| 起始物质的量 | n(SO2)/mol | 0.40 | 0.80 | 0.80 | 0.40 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
| SO2的平衡转化率% | 80 | α1 | α2 | α3 | |
| A. | 甲中反应的平衡常数小于乙 | |
| B. | 该温度下,该反应的平衡常数K为400 | |
| C. | SO2的平衡转化率:α1>α2=α3 | |
| D. | 容器中SO3的物质的量浓度:丙=丁<甲 |
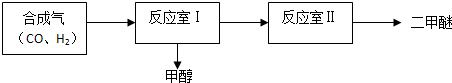
反应室Ⅰ:CO(g)+2H2(g)═CH3OH(g)
反应室Ⅱ:2CH3OH(g)═CH3OCH3(g)+H2O(g)
(1)欲提高反应室Ⅰ中CO的转化率,可以采取的方法有增大氢气浓度、不断分离出甲醇或者加压.
(2)反应室Ⅰ(恒容10L)中有关反应数据如下:
| 序号 | 温度(°C) | 起始浓度(mol•L-1) | 平衡浓度(mol•L-1) | ||||
| CO | H2 | CH3OH | CO | H2 | CH3OH | ||
| ① | T | 1 | 3 | 0 | 0.2 | 1.4 | 0.8 |
| ② | T | 1.5 | 4.6 | 0.1 | b1 | b2 | b3 |
| ③ | T+30 | 1 | 3 | 0 | 0.25 | 1.5 | 0.75 |
②判断:$\frac{{b}_{3}}{{b}_{1}}$>4(填“>”、“<”或“=”).
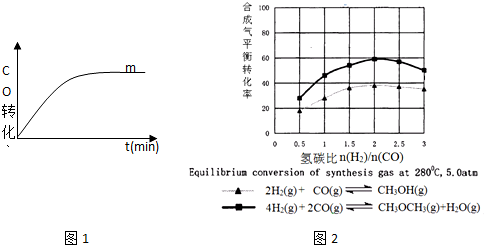
(3)图2表示甲醇或二甲醚体积分数随氢碳比$\frac{n({H}^{2})}{n(CO)}$的变化情况,从图中可以得到的结论是C.
A.提高氢碳比可以加快反应速率
B.提高氢碳比可以提高氢气的转化率
C.按方程式系数比投料时甲醇或二甲醚体积分数最大
D.对于同一反应氢碳比越大,生成物浓度越大
(4)已知某温度下下列热化学方程式:CO(g)+2H2(g)═CH3OH(g)△H1=-100.46kJ•mol-1
2CH3OH(g)═CH3OCH3(g)+H2O(g)△H2=-20.59kJ•mol-1,则2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g)△H3=-221.51kJ•mol-1.

(2)如图 II表示50mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)D.
A.是a mL B.是(50-a)mLC.一定大于a mL D.一定大于(50-a)mL
(3)某研究性学习小组为了探究醋酸的电离情况,进行了如实验.配制并标定醋酸溶液的浓度,取冰醋酸配制250mL 0.2mol•L-1的醋酸溶液,用0.2mol•L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定.回答下列问题:
①配制250mL 0.2mol•L-1醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和250 mL容量瓶.
②为标定某醋酸溶液的准确浓度,用0.200 0mol•L-1的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如表:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
③关于该滴定实验,从下列选项中选出最恰当的一项D(选填字母).
| 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 | |
| A | 碱 | 酸 | 石蕊 | (乙) |
| B | 酸 | 碱 | 甲基橙 | (甲) |
| C | 碱 | 酸 | 酚酞 | (甲) |
| D | 酸 | 碱 | 酚酞 | (乙) |
用pH计测定25℃时不同浓度的醋酸的pH,结果如表:
| 醋酸浓度(mol•L-1) | 0.001 0 | 0.010 0 | 0.020 0 | 0.100 0 | 0.200 0 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
④根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是:0.0100 mol•L-1醋酸的pH大于2或醋酸稀释10倍时,pH的变化值小于1.
⑤从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度将增大.(填“增大”“减小”或“不变”)
探究温度对醋酸电离程度的影响
⑥请你设计一个实验完成该探究,请简述你的实验方案:用pH计(或精密pH试纸)测定相同浓度的醋酸在几种不同温度时的pH.