题目内容
北京奥运会“祥云”火炬燃料是丙烷(![]() ),亚特兰大奥运会火炬燃料是丙烯 (
),亚特兰大奥运会火炬燃料是丙烯 (![]() )。
)。
(1)丙烷脱氢可得丙烯。
已知:![]()
![]()
![]()
![]()
![]()
![]()
则相同条件下,反应![]() 的
的![]() =
= ![]()
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入![]() 和
和![]() ,负极通入丙烷,电解质是熔融碳酸盐。电池反应方程式为 ;放电时,
,负极通入丙烷,电解质是熔融碳酸盐。电池反应方程式为 ;放电时,![]() 移向电池的 (填 “正”或“负”)极。
移向电池的 (填 “正”或“负”)极。
(3)碳氢化合物完全燃烧生成![]() 和
和![]() 。常温常压下,空气中的
。常温常压下,空气中的![]() 溶于水.达到平衡时,溶液的pH=5.60,c(
溶于水.达到平衡时,溶液的pH=5.60,c(![]() )=1.5×10-5mol?L-1。若忽略水的电离及
)=1.5×10-5mol?L-1。若忽略水的电离及![]() 第二级电离,则
第二级电离,则![]()
![]()
![]() 的平衡常数
的平衡常数![]() (已知:10-5.60=2 5×10-6)
(已知:10-5.60=2 5×10-6)
(4)常温下,0.l mol? L-1![]() ,溶液的pH大于8.则溶液中c(
,溶液的pH大于8.则溶液中c(![]() ) c(
) c(![]() )(填、“>” “=”或 “<” ,原因是 (用离子方程式和必要的文字说明)。
)(填、“>” “=”或 “<” ,原因是 (用离子方程式和必要的文字说明)。
(1)124.2
(2)![]() ====
====![]() 负
负
(3)4.2![]()
(4)![]()
![]()
![]()
![]() (或
(或![]()
![]()
![]() )
)
![]()
![]()
![]()
![]() 的水解程度大于电离程度
的水解程度大于电离程度

练习册系列答案
相关题目
 HCO3-+H+的平衡常数K1=
HCO3-+H+的平衡常数K1= CO32-+H+,HCO3-+H2O
CO32-+H+,HCO3-+H2O H2CO3+OH-,
H2CO3+OH-,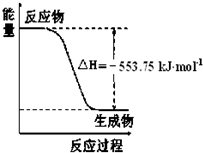 (1)盖斯定律认为:不管化学过程是一步完成或分数步完成,整个过程的总
(1)盖斯定律认为:不管化学过程是一步完成或分数步完成,整个过程的总