题目内容
11.乙苯是一种用途广泛的有机原料,可制备多种化工产品.(一)制备苯乙烯(原理如反应I所示):
I.
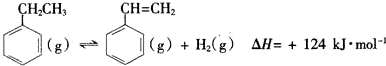
(1)部分化学键的键能如表所示:
| 化学键 | C-H | C-C | C=C | H-H |
| 键能/kJ•mol-1 | 412 | 348 | x | 436 |
(2)工业上,在恒压设备中进行反应I时,常在乙苯蒸气中通入一定量的水蒸气.用化学平衡理论解释通入水蒸气的原因为该反应正向为气体分子数增大的反应,入水蒸气需增大容器容积,减小体系压强,平衡正向移动,增大反应物的转化率.
(3)从体系自由能变化的角度分析,反应I在高温(填“高温”或“低温”)下有利于其自发进行.
(二)制备α-氯乙基苯(原理如反应II所示):
II.
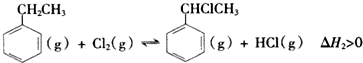
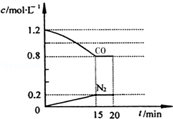
(4)T℃时,向10L恒容密闭容器中充人2mol乙苯(g)和2mol Cl2(g)发生反应Ⅱ,5min时达到平衡,乙苯和Cl2、α-氯乙基苯和HCl的物质的量浓度(c)随时间(t)变化的曲线如图l所示:
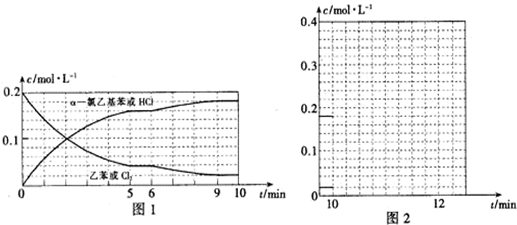
①0-5min内,以HCl表示的该反应速率v(HCl)=0.032 mol•L-1•min-1.
②T℃时,该反应的平衡常数K=16.
③6min时,改变的外界条件为升高温度.
④10min时,保持其他条件不变,再向容器中充人1moI乙苯、1mol Cl2、1mol α-氯乙基苯和l mol HCl,12min时达到新平衡.在图2中画出10-12min,Cl2和HCl的浓度变化曲线(曲线上标明Cl2和HC1);0-5min和0-12min时间段,Cl2的转化率分别用α1、α2表示,则αl<α2(填“>”、“<”或“=”).
分析 (1)反应热=反应物总键能-生成物总能键能,由有机物的结构可知,应是-CH2CH3中总键能与-CH=CH2、H2总键能之差;
(2)保持压强不变,加入水蒸气,容器体积应增大,等效为降低压强,平衡向气体体积增大的方向移动;
(3)G=△H-T△S,△G为自由能变化,△H为焓变,T为热力学温度,△S熵变.当△G<0时反应能自发进行,△G>0时反应不能自发进行,据此分析判断;
(4)①根据v=$\frac{△n}{\frac{V}{△t}}$计算;
②化学平衡常数为生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比值,利用三段式计算平衡常数;
③6min时,反应向正反应方向移动;根据影响平衡移动的条件可知,改变的外界条件为升高温度;
④10min时,计算平衡常数,保持其他条件不变,再向容器中充人1moI乙苯、1mol Cl2、1mol α-氯乙基苯和l mol HCl,相当于增加反应物的浓度,平衡正向移动,12min时达到新平衡,平衡常数不变,利用三段式计算并画图.
解答 解:(1)反应热=反应物总键能-生成物总能键能,由有机物的结构可知,应是-CH2CH3中总键能与-CH=CH2、H2总键能之差,设C=C键能为X,则△H=(5×412+348-3×412-X-436)kJ•mol-1=124kJ•mol-1,解得X=612KJ/mol;
故答案为:612KJ/mol;
(2)降低压强,平衡向体积增大的方向移动,制备苯乙烯的正反应为气体分子数增大的反应,保持压强不变,加入水蒸气,容器体积应增大,等效为降低压强,平衡向正反应方向移动,提高乙苯的平衡转化率;
故答案为:正反应为气体分子数增大的反应,保持压强不变,加入水蒸气,容器体积应增大,等效为降低压强,平衡向正反应方向移动,提高乙苯的平衡转化率;
(3)反应自发进行需要满足,△H-T△S<0,依据题干条件可知,制备苯乙烯的正反应为气体分子数增大的反应,△S>0,正反应吸热,△H=+124KJ/mol>0,所以反应一定是在高温条件下才能自发进行,
故答案为:高温;
(4)①T℃时,向10L恒容密闭容器中充人2mol乙苯(g)和2mol Cl2(g)发生反应Ⅱ,5min时达到平衡,依据题干条件可知,C(HCl)=0.16mol/L,v=$\frac{△n}{\frac{V}{△t}}$=$\frac{0.16mol/L}{5min}$=0.032 mol•L-1•min-1,
故答案为:0.032 mol•L-1•min-1;
② 5min时达到平衡,依据题干条件可知,C(HCl)=0.16mol/L,n(HCl)=1.6mol,
5min时达到平衡,依据题干条件可知,C(HCl)=0.16mol/L,n(HCl)=1.6mol,
起始(mol) 2 2 0 0
转化(mol) 1.6 1.6 1.6 1.6
平衡(mol) 0.4 0.4 1.6 1.6 平衡常数为K=$\frac{\frac{1.6}{10}×\frac{1.6}{10}}{\frac{0.4}{10}×\frac{0.4}{10}}$=16,
故答案为:16;
③制备α-氯乙基苯的正反应为吸热反应,反应前后气体的体积不变,6min时,乙苯、Cl2的浓度在减小,而α-氯乙基苯和HCl的浓度在增加,反应向正反应方向移动,只能是升高温度,
故答案为:升高温度;
④10min时,乙苯、Cl2、α-氯乙基苯和 HCl的物质的量浓度分别为:0.02mol/L、0.02mol/L、0.18mol/L、0.18mol/L,平衡常数为K=$\frac{0.18×0.18}{0.02×0.02}$=81,此时乙苯、Cl2、α-氯乙基苯和 HCl的物质的量浓度比为:1:1:9:9,保持其他条件不变,再向容器中充人1mol 乙苯、1mol Cl2、1mol α-氯乙基苯和l mol HCl,相当于增加反应物的浓度,平衡正向移动,则α1<α2,设转化的乙苯物质的量浓度为x,则
起始(mol/L) 0.12 0.12 0.28 0.28
转化(mol/L) x x x x
平衡(mol/L) 0.12-x 0.12-x 0.28+x 0.28+x
平衡常数为K=$\frac{(0.28+x)×(0.28+x)}{(0.12-x)×(0.12-x)}$=81,解得x=0.08mol/L,则12min时,乙苯、Cl2物质的量浓度都为0.12-x=0.04mol/L,α-氯乙基苯和 HCl的物质的量浓度都为:0.28+x
=0.36mol/L,浓度变化曲线如图: ,
,
故答案为:<; .
.
点评 本题考查了反应热的计算、化学平衡理论,明确应热=反应物总键能-生成物总能键能,熟悉影响化学平衡移动的因素是解题关键,注意(4)利用平衡常数不变,利用三段式计算并画图是该题的难点,题目难度中等.

| 压强/MPa | 10 | 20 | 30 | 40 |
| φ(NH3) | 0.30 | 0.45 | 0.54 | 0.60 |
| A. | 10 MPa时,H2的转化率为75% | |
| B. | 20 MPa时,NH3的物质的量浓度是10 MPa时的1.5倍 | |
| C. | 40 MPa时,若容器的体积为VL,则平衡常数$K=\frac{{64{V^2}}}{3}$ | |
| D. | 30 MPa时,若向容器中充入惰性气体,则平衡向正反应方向移动 |
 向容积固定的容器甲和带有活塞的定压容器乙中分别通入2mol SO2和1mol O2(如下图),若开始通气时两容器的体积相同,在相同温度下反应,一段时间后,反应达到平衡.则下列说法正确的是( )
向容积固定的容器甲和带有活塞的定压容器乙中分别通入2mol SO2和1mol O2(如下图),若开始通气时两容器的体积相同,在相同温度下反应,一段时间后,反应达到平衡.则下列说法正确的是( )| A. | 平衡时,两容器内SO3的浓度必定相等 | |
| B. | 平衡时,混合气体中的SO3的体积分数甲比乙高 | |
| C. | SO2的转化率乙容器内比甲容器内高 | |
| D. | 反应后的相同时间内,甲容器中的反应速率大 |

 回答下列问题:
回答下列问题: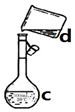 (1)现需配制0.1mol/LNaOH溶液500mL,装置是某同学转移溶液的示意图
(1)现需配制0.1mol/LNaOH溶液500mL,装置是某同学转移溶液的示意图