题目内容
Ⅰ:从①渗析、②聚沉、③丁达尔效应 ④凝胶、⑤布朗运动、⑥电泳.中选出适当的序号填入下列每小题后面的空格中:(注意:填序号)
(1)用半透膜把制取的Fe(OH)3胶体中生成的氯化钠分离的方法叫做 .
(2)在肥皂水中透过强光,可见到光带,这种现象称为 .
(3)在Fe(OH)3胶体中加入(NH4)2SO4,产生红褐色沉淀,这种现象叫做 .
(4)在水泥厂和冶金厂常用高压电对气溶胶作用,除去大量烟尘,以减小对空气的污染.这种做法应用的主要原理是 .
Ⅱ:同温同压下,同体积的氨气和硫化氢气体(H2S)的质量比为 ; 同质量的氨气和硫化氢气体的体积比为 ,其中含有的氢的原子个数比为 ;若二者氢原子数相等,它们的体积比为 .
(1)用半透膜把制取的Fe(OH)3胶体中生成的氯化钠分离的方法叫做
(2)在肥皂水中透过强光,可见到光带,这种现象称为
(3)在Fe(OH)3胶体中加入(NH4)2SO4,产生红褐色沉淀,这种现象叫做
(4)在水泥厂和冶金厂常用高压电对气溶胶作用,除去大量烟尘,以减小对空气的污染.这种做法应用的主要原理是
Ⅱ:同温同压下,同体积的氨气和硫化氢气体(H2S)的质量比为
考点:胶体的重要性质,物质的量的相关计算
专题:计算题,溶液和胶体专题
分析:Ⅰ(1)胶粒不能透过半透膜;
(2)光束通过胶体时,产生光亮的通路,称为丁达尔效应;
(3)胶粒遇电解质溶液发生聚沉;
(4)胶粒在电场的作用下,做定向运动,这种现象称为电泳;
Ⅱ同温同压下,同体积的气体物质的量相同,气体的质量之比等于相对分子质量之比;
根据质量计算物质的量,气体的体积之比等于物质的量之比;
根据物质的量和分子的组成判断氢原子数目之比;
根据分子组成计算氢原子数相等时物质的量关系,进而计算体积之比.
(2)光束通过胶体时,产生光亮的通路,称为丁达尔效应;
(3)胶粒遇电解质溶液发生聚沉;
(4)胶粒在电场的作用下,做定向运动,这种现象称为电泳;
Ⅱ同温同压下,同体积的气体物质的量相同,气体的质量之比等于相对分子质量之比;
根据质量计算物质的量,气体的体积之比等于物质的量之比;
根据物质的量和分子的组成判断氢原子数目之比;
根据分子组成计算氢原子数相等时物质的量关系,进而计算体积之比.
解答:
解:Ⅰ(1)胶粒不能透过半透膜,离子能透过,可用渗析提纯胶体,故答案为:①.
(2)肥皂水的分散系为胶体,有丁达尔效应,故答案为:③;
(3)Fe(OH)3胶体遇到(NH4)2SO4发生聚沉,故答案为:②;
(4)胶粒在电场的作用下,做定向运动,这种现象称为电泳,可用来除尘,故答案为:⑥;
Ⅱ解答:根据阿伏加德罗定律定律,相同条件下,相同体积的任何气体都含有相同的数目的粒子,
则同温同压下,同体积的气体物质的量相同,根据m=n?M可知,
气体的质量之比等于相对分子质量之比,所以同温同压下,同体积的氨气和硫化氢气体(H2S)的质量比为17:34=1:2;
设氨和硫化氢气体的质量分别为34g,则n(NH3)=
=2mol,n(H2S)=1mol,
相同条件下,物质的越多,气体的体积越大,则同质量的氨和硫化氢气体的体积比为2:1;
2molNH3中H原子的个数为:2mol×3×NA/mol=6NA,
1molH2S中H原子的个数为:1mol×2×NA/mol=2NA,
其中含有的氢的原子个数比为:6:2=3:1;
若二者氢原子数相等,设含有6molH原子,则
氨气的物质的量为2mol,硫化氢的物质的量为3mol,
则体积之比为2:3.
故答案为:1:2;2:1;3:1;2:3.
(2)肥皂水的分散系为胶体,有丁达尔效应,故答案为:③;
(3)Fe(OH)3胶体遇到(NH4)2SO4发生聚沉,故答案为:②;
(4)胶粒在电场的作用下,做定向运动,这种现象称为电泳,可用来除尘,故答案为:⑥;
Ⅱ解答:根据阿伏加德罗定律定律,相同条件下,相同体积的任何气体都含有相同的数目的粒子,
则同温同压下,同体积的气体物质的量相同,根据m=n?M可知,
气体的质量之比等于相对分子质量之比,所以同温同压下,同体积的氨气和硫化氢气体(H2S)的质量比为17:34=1:2;
设氨和硫化氢气体的质量分别为34g,则n(NH3)=
| 34g |
| 17g/mol |
相同条件下,物质的越多,气体的体积越大,则同质量的氨和硫化氢气体的体积比为2:1;
2molNH3中H原子的个数为:2mol×3×NA/mol=6NA,
1molH2S中H原子的个数为:1mol×2×NA/mol=2NA,
其中含有的氢的原子个数比为:6:2=3:1;
若二者氢原子数相等,设含有6molH原子,则
氨气的物质的量为2mol,硫化氢的物质的量为3mol,
则体积之比为2:3.
故答案为:1:2;2:1;3:1;2:3.
点评:本题考查胶体的性质、物质的量的有关计算以及阿伏加德罗定律及推论的应用,题目难度不大,注意物质的量与质量、体积、微粒数目之间的计算公式的运用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
对于Cl2+SO2+2H2O═H2SO4+2HCl反应,下列说法正确的是( )
①Cl2是氧化剂 ②SO2被氧化 ③Cl2被氧化 ④Cl2发生还原反应 ⑤SO2具有还原性 ⑥Cl2具有氧化性.
①Cl2是氧化剂 ②SO2被氧化 ③Cl2被氧化 ④Cl2发生还原反应 ⑤SO2具有还原性 ⑥Cl2具有氧化性.
| A、只有①②⑥ |
| B、只有②③④ |
| C、只有②④⑤⑥ |
| D、只有①②④⑤⑥ |
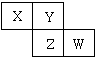 如图是元素周期表的一部分.X、Y、Z、W均为短周期元素,若W原子最外电子层电子数是其内层电子数的
如图是元素周期表的一部分.X、Y、Z、W均为短周期元素,若W原子最外电子层电子数是其内层电子数的| 7 |
| 10 |
| A、X元素的氢化物水溶液呈碱性 |
| B、气态氢化物的稳定性:Y>Z |
| C、最高氧化物对应水化物的酸性:W>Z |
| D、阴离子半径从大到小排列的顺序:Y>Z>W |